下列装置和操作能达到实验目的的是( )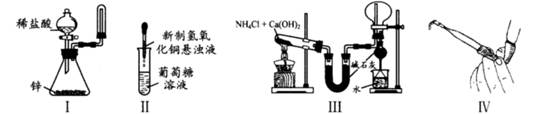
| A.实验I:制取并收集氢气 |
| B.实验II:验证葡萄糖的还原性 |
| C.实验III:实验室制氨气并收集干燥的氨气 |
| D.实验Ⅳ:检查碱式滴定管是否漏液 |
制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
Si(粗)+3HCl(g)  SiHCl3(g) + H2、②SiHCl3 (g) + H2
SiHCl3(g) + H2、②SiHCl3 (g) + H2 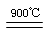 Si(纯) + 3HCl(g)
Si(纯) + 3HCl(g)
对上述两个反应的叙述错误的是
| A.两个反应互为可逆反应 | B.都是置换反应 |
| C.都是氧化还原反应 | D.都不是离子反应 |
下列各组顺序的排列不正确的是
| A.离子半径:Na+>Mg2+>Al3+>F— |
| B.热稳定性:HCl>H2S>PH3 |
| C.酸性强弱:Al(OH)3<H2SiO3<H2CO3<H3PO4 |
| D.熔点:SiO2>NaCl>Na>CO2 |
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10 L密闭容器中进行,10s后,水蒸气的物质的量增加了0.60 mol,则此反应的平均速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为
4NO(g)+6H2O(g)在10 L密闭容器中进行,10s后,水蒸气的物质的量增加了0.60 mol,则此反应的平均速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为
| A.υ(NH3)=0.0060 mol/(L·s) |
| B.υ(NO)=0.0040 mol/(L·s) |
| C.υ(O2)=0.0060 mol/(L·s) |
| D.υ(H2O)=0.036 mol/(L·min) |
几种短周期元素的原子半径及主要化合价如下表
| 元素代号 |
L |
M |
X |
R |
T |
| 原子半径(nm) |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列说法正确的是
A.L、T形成的简单离子核外电子数相等
B.R的氧化物对应的水化物呈强碱性
C.X单质在氧气中燃烧生成XO3
D.离子半径大小:r(M3+)> r(T2-)
下列关于化学键的说法中不正确的是
| A.化学键是一种作用力 |
| B.化学键可以使离子相结合,也可以使原子相结合 |
| C.分子间作用力又称范德华力,它属于化学键 |
| D.化学反应过程中,反应物分子内的化学键断裂,生成物分子中的化学键形成 |