(15分)
呋喃酚是合成农药的重要中间体,其合成路线如下: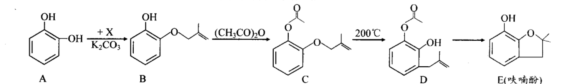
(1)B→C的反应类型是 ;E中含有的官能团名称是 。
(2)已知X的分子式为C4H7C1,写出A→B的化学方程式:
(3)Y是X的同分异构体,分子中无支链且不含甲基,则Y的名称(系统命名)是
(4)下列有关化合物C、D的说法正确的是 (填代号)。
A.可用氯化铁溶液鉴别C和D B.C、D含有的官能团完全相同
C.C、D互为同分异构体 D.C、D均能使溴水褪色
(5)E的同分异构体很多,写出符合下列条件的芳香族同分异构体的结构简式:
①苯环上的一氯代物只有一种 ②含有酯基 ③能发生银镜反应
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第周期族;最高价氧化物的化学式为,砷酸钠的化学式是。
(2)已知下列元素在周期表中的位置,写出它们价电子排布式和元素 符号:
符号:
①第4周期ⅣB族 ;
;
②第5周期ⅦA族。
(8分) 将一定质量的Al、Fe混合物加入到足量的盐酸中,充分反应后得到标准状况下的氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气6.72L。
(1)写出与碱反应涉及的化学方程式:_____________________________________
(2)混合物中Al和Fe的质量分别为________和__________
(3)当混合物与盐酸反应时,转移电子数为_______mol;与NaOH溶液反应时转移电子
数为_______mol。
A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3—、SO42—、Cl—、SO32—的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四只试管中,只有C盐的溶液呈蓝色。
②若向①的四只试管中分别加盐酸,B盐溶液有沉淀产生,D盐溶液有刺激性气体逸出。根据实验事实可推断它们的化学式为:
A_________、B_________、C_________、D____________
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示。
请回答:
(1)写出B物质的化学式:;F的名称:。
(2)写出第③步反应的化学方程式为。
(3)第④步反应中溶液颜色的变化;
写出第④步反应的离子方程式。
(4)写出SO2和B反应的离子方程式。
(5)F溶液中滴入NaOH溶液可能产生的实验现象是。
(共 11 分)
(1)有一种叫做钾长石(K2Al2Si6O16),其化学式为写成氧化物的形式为______________
(2)反应3Cu+8HNO3 = 3Cu(NO3)2+2NO↑+4H2O 的离子方程式为:
每生成11.2L标准状况下的气体,被还原的(填名称)的质量为 g。
得电子与失电子个数比是_____,被氧化与被还原的原子的个数比为______,试用“单线桥”标出该反应电子转移方向和数目:_____________________________ (3)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
(3)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
① A + H2O → B + C② C + F → D③ D + NaOH → F + E + H2O
写出A 、B、 C的化学式A______ B ____ C______
写出反应③的离子方程式