SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是
| A.Na2SO3溶液中存在:c(Na+)>c(SO32-)>c(H2SO3)>c(HSO3-) |
| B.已知NaHSO3溶液pH<7,该溶液中:c(Na+)>c(HSO3-)>c(H2SO3) >c(SO32-) |
| C.当吸收液呈中性时:c(Na+)=2 c(SO32-)+c(HSO3-) |
| D.当吸收液呈酸性时:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
下列推断正确的是
| A.SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物 |
| B.Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同 |
| C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D.新制氯水显酸性,向其中滴加少最紫色石蕊试液,充分振荡后溶液呈红色 |
下列说法中不正确的是
| A.液氨、液态氯化氢都是电解质 |
| B.Na2O2、HClO、SO2等物质都具有漂白作用 |
| C.置换反应都是氧化还原反应,复分解反应都是非氧化还原反应 |
| D.明矾能水解生成氢氧化铝胶体,可用作净水剂 |
向100mL pH=0的硫酸和硝酸混合溶液中投入3.84g铜粉,微热使反应充分完成后,生成NO气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为
| A.0.02mol | B.0.08mol | C.0.10mol | D.0.16mol |
在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g)  nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是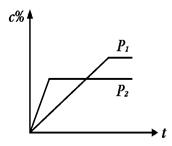
| A.P1>P2,n<3 | B.P1<P2,n>3 |
| C.P1>P2,n>3 | D.P1<P2,n<3 |
Na2CO3水溶液中存在CO2-3+H2O HCO-3+OH-平衡。下列说法不正确的是
HCO-3+OH-平衡。下列说法不正确的是
A.稀释溶液,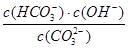 增大 增大 |
| B.通入CO2,溶液pH减小 |
| C.升高温度,此平衡常数增大 |
D.加入NaOH固体,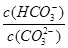 减小 减小 |