科学地补充碘可防止碘缺乏病。
(1)上图为海带制碘的流程图。步骤③的实验操作中用到的玻璃仪器除了烧杯、玻璃棒之外还有 ;当步骤④反应中转移0.2mol电子时生成碘的质量:
(2)碘酸钾(KIO3)是食盐的加碘剂。KIO3在酸性介质中能与H2O2或I-作用均生成单质碘。
请回答下列问题:
①以碘为原料,通过电解制备碘酸钾的实验装置如图所示。电解前,将一定量的精制碘溶于过量氢氧化钾溶液,溶解是发生反应为:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区。电解时,阳极反应: I-+6OH--6e-=IO3-+3H2O,当外电路上通过3mol电子时(碘离子被完全消耗),溶液中的IO3-的物质的量是 ;阴极上产生的气体在标准状况下的体积: 。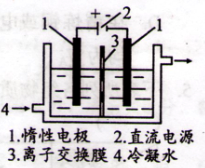
②电解过程中,需通过检验阳极电解液中是否有I-存在以确定电解是否完成。请设计判断电解是否完成的实验方案,并填人下表。仪器不限,可选的试剂:淀粉溶液、H2O2溶液、稀硫酸。
| 实验操作 |
实验现象及结论 |
| |
|
科学家通过乙二醇的桥梁作用把阿司匹林连接在高聚物上,制成缓释长效阿司匹林,用于关节炎和冠心病的辅助治疗,缓释长效阿司匹林的结构简式如下: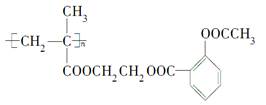
试填写以下空白:
(1)高分子载体结构简式为________。
(2)阿司匹林连接在高分子载体上的有机反应类型是________________。
(3)缓释长效阿司匹林在肠胃中变为阿司匹林的化学方程式是______________________。
高分子纤维E广泛用于通讯、导弹、宇航等领域,可用芳香烃A为原料来合成,合成路线如下: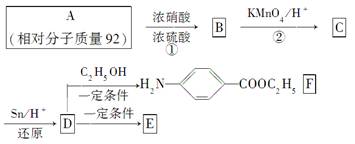
请回答:
(1)写出结构简式:A__________,B____________,
C____________。
(2)写出反应类型:①__________,②_______________________________。
(3)写出D→E聚合的化学方程式___________________。
(4)下列化合物中能与F发生化学反应的是________。
a.HCl b.NaClc.Na2CO3 d.NaOH
卤代烃分子中的卤原子与活泼金属阳离子结合,发生下列反应:
根据下列物质的转化关系,回答下列问题:
(1)A的分子式是________,E的结构简式是________。
(2)B→D的化学方程式(不必注明反应条件)__________________________ ________。
(3)C→F的化学方程式(不必注明反应条件)_______________________ _____________。
11 mol丙酮酸 在镍催化剂作用下加1 mol氢气转化变成乳酸。乳酸的结构简式为_________________________________________。
在镍催化剂作用下加1 mol氢气转化变成乳酸。乳酸的结构简式为_________________________________________。
2与乳酸具有相同官能团的乳酸的同分异构体A在酸性条件下,加热失水生成B,由A生成B的化学反应方程式是_________________________________
3B的甲酯可以聚合,聚合物的结构简式是 。
人造羊毛的主要成分为 ,此物质可由以下三种途径合成,已知A是石油分馏的一种产品。
,此物质可由以下三种途径合成,已知A是石油分馏的一种产品。
回答下列问题:
1写出A的分子式________________,D的结构简式__________________
2在反应①~⑥中,属于加成反应的是
3写出反应⑥的化学方程式:_____________________________________
4从能源和环保的角度看,你认为最有发展前景的是 ,其中理由是____________________________________________________