下列大小关系比较正确的是
| A.离子半径:F-<Na+<Mg2+ |
| B.电负性:C<O<N |
| C.氢化物的沸点:NH3<PH3<AsH3 |
| D.碱性: NaOH>Mg(OH)2> Al(OH)3 |
下列离子方程式书写正确的是( )
| A.向NaHSO4溶液中滴加Ba(OH)2溶液显中性:H++SO42-+Ba2++OH-==BaSO4↓+H2O | |
| B.向NaAlO2溶液中加盐酸至呈酸性:AlO2-+4H+==Al3++2H2O | |
C.碳酸氢铵溶液中加入过量NaOH:HCO3-+OH-==CO32-+H2O |
D.向苯酚钠溶液中通入过量CO2:2 -O-+CO2+H2O → 2-OH+CO32- -O-+CO2+H2O → 2-OH+CO32- |
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、NH4+、Fe3+、A13+、Cl―、OH―、NO3―、S2―、CO32―、SO42―。已知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是()
| A.OH―、CO32―、SO42― | B.S2―、Cl―、SO42― |
| C.CO32―、NO3―、S2― | D.Cl―、SO42―、NO3― |
常温时,某溶液中由水电离出的H+和OH-的物质的量浓度乘积为1×10-26,该溶液中一定能大量存在的离子组是()
| A.K+、Ba2+、Cl-、NO3- | B.Fe3+、Cu2+、Cl-、HCO3- |
| C.K+、Na+、SO32-、SO42- | D.Ca2+、Al3+、H+、NO3- |
下列反应对应的离子方程式正确的是()
A.铜与硝酸银溶液反应: |
B.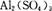 溶液中加入过量氨水: 溶液中加入过量氨水: |
C.氢氧化钡溶液和稀硫酸反应: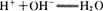 |
D.用惰性电极电解CuCl2溶液: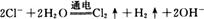 |
下列反应的离子方程式正确的是( )
| A.氢氧化钠溶液中通入少量二氧化硫:SO2+OH- = HSO3- |
| B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3- +Ba2++OH- = BaCO3↓+H2O |
| C.盐酸滴入氨水中:H-+OH- = H2O |
| D.碳酸钙溶解于稀硝酸中:CO32 -+2H+ = CO2↑+H2O |