合成氨工业、硫酸工业的生产工艺流程大致为:
合成塔和接触室中的反应分别为:N2(g)+3H2(g)  2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)  2SO3(g) △H﹤0
2SO3(g) △H﹤0
(1)写出流程中设备的名称:B ,X 。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是 。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是 (填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是 。
(5)工业生产中常用氨——酸法进行尾气脱硫,以达到消除污染、废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是 。
下列各组离子在指定溶液中一定能大量共存的是( )
| A.在能使石蕊试纸变蓝色的溶液中:Na+、AlO2-、S2-、SO42- |
B.由水电离出的c(H+)=10-12mol·L-1的溶液中:Cl-、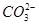 、NH4+、SO32 、NH4+、SO32 |
C.在加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、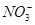 |
| D.pH=2的溶液中:Na+、SO42-、ClO-、SO32 |
下列离子方程式错误的是()
| A.向FeBr2溶液中通入少量的Cl2 2Fe2+ + Cl2 = 2Fe3+ + 2Cl- |
| B.向FeBr2溶液中通入与FeBr2等物质的量的Cl2 2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl- |
| C.向FeBr2溶液中通入足量的Cl2 2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl- |
| D.向苯酚钠溶液中通入“少量”的CO2 |
2 -O-+CO2+H2O→2
-O-+CO2+H2O→2 -OH↓+CO32-
-OH↓+CO32-
下列说法正确的是 ( )
| A.HR溶液导电性较弱,HR属于弱电解质 |
| B.某化合物溶解于水导电,则该化合物为电解质 |
| C.根据电解质在其水溶液中能否完全电离,将电解质分成强电解质与弱电解质 |
| D.食盐是电解质,食盐的水溶液也是电解质 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,15 g甲基(-CH3)所含的电子数为7NA |
| B.水的摩尔质量就是NA个水分子的质量之和 |
| C.含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D.1 mo1Mg与足量O2或N2反应生成MgO或Mg3 N2均失去2NA个电子 |
设NA代表阿伏加德罗常数的数值,则下列说法正确的是
| A.1.8 g D2O含有NA个中子 |
| B.用5 mL 3 mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
| C.在Na2O2与CO2的反应中,每转移NA个电子时,消耗22.4 L的CO2 |
| D.25℃时,7 g C2H4和C3H6的混合气体中,含有NA个C-H键 |