水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH—
+O2+xOH— Fe3O4+S4O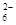 +2H2O,
+2H2O,
下列说法中,正确的是( )
| A.每生成1mol Fe3O4,反应转移的电子总数为3mol ; |
| B.x="6" |
| C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol; |
| D.Fe2+和S2O32—-都是还原剂; |
实验室制浓硫酸、浓硝酸的混合物与苯反应制取硝基苯。得到粗产品后,要选用如下几步操作对粗产品进行精制:①蒸馏 ②水洗 ③用干燥剂进行干燥 ④用10%的NaOH溶液洗涤。正确的操作步骤是
| A.①②③④② | B.②④②③① | C.④②③①② | D.③④①②③ |
研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们视为一种潜在的清洁燃料。液氨燃烧的化学反应方程式为:4NH3+3O2 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
| 燃料 |
沸点(℃) |
燃烧热(kJ/mol) |
相对分子质量 |
液态密度(g/cm3) |
| 氢 |
-252.6 |
238.40 |
2.02 |
0.07 |
| 氨 |
-33.50 |
317.10 |
17.03 |
0.61 |
①以氨和氢为燃料时,可以减缓温室效应
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量多
④氨的液化比氢容易得多
A.①③ B.②③ C.①④ D.②④
在一定条什下,下列有机物都能发生加成反应、取代反应、水解反应和中和反应共四种反应的是
A.一滴香: |
B.芬必得: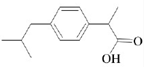 |
C.维生素B5: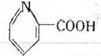 |
D.扑热息痛: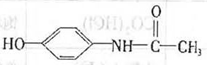 |
下列物质性质的比较,正确的是
| A.热稳定性:Na2CO3>NaHCO3>H2CO3 |
| B.熔点:K>Na>Li |
| C.同条件下,同浓度溶液的pH值:NaHCO3>Na2CO3 |
| D.还原性:S2->Br->I- |
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
| A.两种气体的压强相等 | B.O2比O3质量小 |
| C.两种气体的分子数目相等 | D.两种气体的氧原子数目相等 |