向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这种离子的物质的量随消耗氯气物质的量的变化如图所示。下列说法中正确的是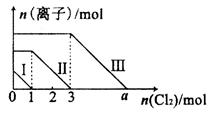
| A.线段III代表Fe2+的变化情况 |
| B.线段I代表Br-的变化情况 |
| C.a值等于6 |
D.原混合溶液中 |
下列反应中,产生氢气速度最快的是()
| A.常温下铝与6mol/L的硝酸 | B.常温下镁与3mol/L的醋酸 |
| C.常温下铁与3mol/L的盐酸 | D.常温下镁与3mol/L的硫酸 |
物质的量浓度相同的下列溶液中,按pH由小到大顺序排列的是()
| A.Na2CO3 NaHCO3 NaCl HCl |
| B.Na2CO3 NaHCO3 HCl NaCl |
| C.(NH4)2SO4 NH4Cl NaNO3 Na2CO3 |
| D.NH4Cl (NH4)2SO4 Na2CO3 NaNO3 |
工业制硫酸中的一步重要反应是SO2在400-500下的催化氧化,2SO2+O2 2SO3,这是一个正反应放热的可逆反应在,如果反应在密闭容器中进行,下述有关说法中错误的是( )
2SO3,这是一个正反应放热的可逆反应在,如果反应在密闭容器中进行,下述有关说法中错误的是( )
| A.使用催化剂是为了加快反应速率. |
| B.在上述条件下SO2不可能100%的转化为SO3 |
| C.为了提高SO2转化率,应适当提高O2浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
下列叙述不正确的是( )
| A.PH相等体积相等的盐酸和醋酸加水稀释10倍后,前者的PH大于后者 |
| B.PH相等体积相等的盐酸和醋酸分别中和0.1mol/L的NaOH溶液,消耗NaOH溶液体积相等 |
| C.等浓度等体积的盐酸和醋酸与足量的锌粉反应,开始时前者产生H2的速率大于后者,最终产生的H2相等。 |
| D.等浓度等体积的盐酸和醋酸分别中和0.1mol/L的NaOH溶液,消耗NaOH溶液体积相等 |
已知在298K时下述反应的有关数据:
C(s)+1/2 O2(g) ="==" CO(g)△H1 = -110.5 kJ• mol-1
C(s)+O2(g) ="==" CO2(g)△H2= -393.5 kJ• mol-1
则C(s)+CO2(g) ="==" 2CO(g) 的△H 为()
| A.+172.5 kJ• mol-1 | B.+283.5 kJ• mol-1 |
| C.-172.5 kJ• mol-1 | D.-504 kJ• mol-1 |