已知反应2D+E 3F+2G,用传感器测得该反应在不同pH条件下,物质D的浓度(用每升溶液所含溶质的质量表示,单位为mg/L)变化如图所示,下列有关说法正确的是
3F+2G,用传感器测得该反应在不同pH条件下,物质D的浓度(用每升溶液所含溶质的质量表示,单位为mg/L)变化如图所示,下列有关说法正确的是
| A.pH=6.8时,D的浓度(mg/L)一定最大 |
| B.在pH相同的条件下,增大压强,D的浓度(mg/L)增大 |
| C.调节pH到8.8,可使该反应正、逆反应速率都为0 |
| D.温度相同时,不同pH条件下,该反应的平衡常数相同 |
下列关于化学反应速率的说法错误的是
| A.化学反应速率是用于衡量化学反应进行快慢的物理量 |
| B.决定化学反应速率的主要因素是反应物本身的性质 |
| C.Al在氧气中燃烧,将Al粉改为Al片可加快反应速率 |
| D.Zn与稀硫酸反应时,适当提高溶液的温度可加快反应速率 |
下列化合物中既有离子键又有共价键的是
| A.NaOH | B.H2S |
| C.CaCl2 | D.H2O2 |
下列化学用语错误的是
A.聚乙烯的结构简式为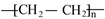 |
| B.淀粉的化学式为(C6H10O5)n |
| C.乙酸的分子式C2H4O2 |
| D.甘氨酸的结构式为C2H5O2N |
下列说法正确的是
| A.液化石油气和天然气的主要成分都是甲烷 |
| B.使用溴水或酸性KMnO4溶液无法鉴别乙烯和甲烷 |
| C.在加热或加入盐的情况下,蛋白质都可发生变性 |
| D.淀粉水解的最终产物是葡萄糖 |
对于反应:2SO2+O2 2SO3,下列说法错误的是
2SO3,下列说法错误的是
| A.使用合适的催化剂可以加大反应速率 |
| B.升高温度可以增大反应速率 |
| C.增大O2浓度可以使SO2转化率达到100% |
| D.增大O2浓度可以增大反应速率 |