设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1 L 1.0 mol/L的NH4Al(SO4)2溶液中含有的氧原子数为8NA |
| B.25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.标准状况下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| D.1 mol FeCl3完全水解得到的Fe(OH)3胶体中含有的胶粒的数目为1NA |
化合物A(C4H8Br2)可由下列反应制得,C4H10O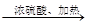 C4H8
C4H8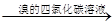 C4H8Br2,则结构式不可能的是
C4H8Br2,则结构式不可能的是
| A.CH3CH(CH2Br)2 | B.CH3CH2CHBrCH2Br |
| C.CH3CHBrCHBrCH3 | D.(CH3)2CBrCH2Br |
下列各组中两个变化所发生的反应,属于同一类型的是
①由甲苯制甲基环己烷、由乙稀制溴乙烷
②乙烯使溴水褪色、乙炔使酸性高锰酸钾水溶液褪色
③由苯制硝基苯、由苯制苯磺酸
| A.只有②③ | B.只有①② | C.只有①③ | D.①②③ |
在室温下,1升某气体分别与4升氧气混和,在引燃后将气体通过浓硫酸,剩余气体回复至室温时体积变为2升,则该气体是①乙烷②乙烯③乙炔④甲烷
| A.只有② | B.只有①②③ | C.只有④ | D.以上均不可能 |
下列化学式所表示的物质一定是纯净物的是
| A.C3 H8 | B.C4H8 | C.C2H6O | D.C7H8 |
某烯烃与氢气加成后得到2,2-二甲基戊烷,烯烃的名称是
| A.2,2-二甲基-3-戊烯 | B.2,2-二甲基-4-戊烯 |
| C.4,4-二甲基-2-戊烯 | D.2,2-二甲基-2-戊烯 |