研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入5 mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法正确的是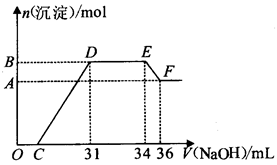
| A.溶液中结合OH-能力最强的离子是NH4+ |
| B.D点时溶液中存在:c(NH4+)+c(H+)=c(OH-)+c(NO3-) |
| C.合金中n(Fe) :n(Al)=1 :3 |
| D.C的值为7 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1mol/L KMnO4溶液:K+、Na+、I-、Cl- |
| B.能溶解Al2O3的溶液:Na+、K+、HCO3-、NO3- |
| C.加入KSCN显红色的溶液:K+、Mg2+、Cl-、SO42- |
| D.水电离出c(OH-)=10-5mol/L的溶液:Na+、Fe2+、Cl-、NO3- |
能正确表示下列反应的离子方程式是
| A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| B.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ |
| C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ |
| D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
不能正确表示下列反应的离子反应方程式为
| A.NH4HCO3溶于过量的浓KOH溶液中:NH4++ HCO3-+2OH-= CO32-+ NH3↑+2H2O |
| B.冷的氢氧化钠溶液中通入氯气 Cl2+ 2OH-=ClO- + Cl-+ H2O |
| C.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| D.醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O |
下列各组离子在指定溶液中一定能大量共存的是
| A.在能使石蕊试纸变蓝色的溶液中:Na+、AlO2-、S2-、SO42- |
| B.由水电离出的c(H+)=10-12mol·L-1的溶液中:Cl-、CO32-、NH4+、SO32 |
| C.在加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3- |
| D.pH=2的溶液中:Na+、SO42-、ClO-、SO32- |
将足量CO2通入下列各溶液中,所含离子还能大量共存的是
| A.K+、SiO32-、Cl-、NO3- |
| B.H+、NH4+、Al3+、SO42- |
| C.Na+、S2-、OH-、SO42- |
| D.Na+、C6H5O-、CH3COO-、HCO3- |