某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是 
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl−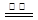 Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,石墨电极附近溶液变红 |
| C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl− |
| D.断开K1,闭合K2时,石墨电极作正极 |
镭是元素周期表中第七周期第ⅡA族元素。下列关于镭的性质描述不正确的是
| A.在化合物中呈+2价 | B.单质能与水反应,放出氢气 |
| C.氢氧化物呈两性 | D.碳酸盐能溶于水 |
设阿伏加德罗常数为NA,下列说法正确的是(Mg-24)
| A.2.4g的Mg粉与足量的盐酸反应失去电子数为0.2NA |
| B.常温常压下,1L0.2mol/L MgCl2溶液中含Cl-数为0.2NA |
| C.常温常压下,22.4L的氧气中含氧原子数为2NA |
| D.18g H2O含有的电子数10NA |
一定量的铝与过量的稀盐酸反应时,为了加快反应速率,但又不影响生成的氢气总量,可以采取的措施是
| A.升高温度 | B.加入适量的水 |
| C.加入少量CuSO4溶液 | D.加入浓度较大的盐酸 |
10mL0.1mol/LAlCl3溶液中,逐滴加入0.1mol/L NaOH溶液v mL,则下列图象正确的是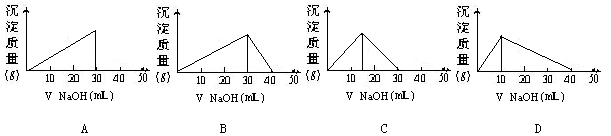
如图所示Cu-Zn原电池,下列叙述正确的是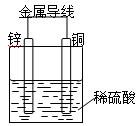
| A.氢离子在负极得电子 |
| B.锌为负极,发生氧化反应 |
| C.铜为负极,铜片上有气泡产生 |
| D.电子从铜极流向锌极 |