氢气既是最理想的能源又是重要的化工原料,用甲烷制氢气是一种廉价的制氢方法。有关的热化学方程式如下: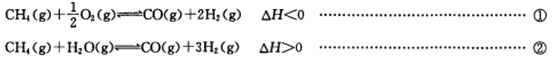
下列说法不正确的是
| A.当反应①中v(CH4)正=v(CO)逆时,表明该反应达平衡状态 |
| B.其他条件不变时,增大体系压强,反应①、②中甲烷的转化率均减小 |
| C.使用高效催化剂可以加快反应速率,同时提高CH4的转化率 |
| D.同一容器内同时发生反应①与②时,容器内温度可能保持不变 |
某元素的原子最外层只有一个电子,它与卤素结合时,所形成的化学键
| A.一定是离子键 | B.一定是共价键 |
| C.可能是离子键也可能是共价键 | D.以上说法都不正确 |
XY2是离子化合物,X和Y的离子的电子层结构与氖原子的相同,则X、Y为
| A.Na和Cl | B.K和S | C.Ca和F | D.Mg和F |
下列各数值表示有关元素的原子序数,其所表示的各原子组中能以共价键相互结合成稳定化合物的是
| A.8与11 | B.9与19 | C.2与19 | D.6与8 |
下列说法中不正确的是
| A.共价化合物中不可能含有离子键 |
| B.阴阳离子之间通过静电引力形成的化学键叫离子键 |
| C.含有共价键的化合物不一定是共价化合物 |
| D.含有离子键的化合物一定是离子化合物 |
下列物质中既含有离子键又含有共价键的是
| A.H2O | B.CaCl2 | C.NaOH | D.Cl2 |