某固体粉末中可能含有KNO3、Cu(NO3)2、AgNO3三种物质中的一种或多种,取一定量该固体粉末,加热后得到A气体a L,将气体用足量水吸收,剩余气体B的体积为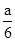 L。下列相关推测错误的是
L。下列相关推测错误的是
| A.气体B可能是O2,也可能是NO |
| B.固体粉末的组成为n(KNO3):n(Cu(NO3)2):n(AgNO3)=1:1:3 |
| C.固体粉末的组成为n(KNO3):n(Cu(NO3)2):n(AgNO3)=1:1:1 |
| D.气体A 中NO2与O2的体积比为9:1 |
某些装饰材料会缓慢释放出某种化学物质,影响健康,这种化学物质可能是
| A.甲醛 | B.O2 | C.N2 | D.CO2 |
下列属于合成高分子材料的是
| A.镁铝合金 | B.水泥 | C.陶瓷 | D.塑料 |
下列反应属于置换反应的是
| A.NH4Cl = NH3↑+ HCl↑ | B.NaCl + AgNO3 =" AgCl↓+" NaNO3 |
| C.CaO + CO2 = CaCO3 | D.Mg + 2HCl = MgCl2 + H2↑ |
下列气体不能用浓H2SO4干燥的是
| A.Cl2 | B.NH3 | C.H2 | D.O2 |
人生病时要合理用药,下列药品与其作用匹配的是
| A.氢氧化铝:中和过多胃酸 | B.阿司匹林:消炎抗菌 |
| C.青霉素:解热镇痛 | D.医用碘酒:人体补碘 |