对含微量I-的某样品进行I-化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用Na2S2O3标准溶液滴定以求得I-的浓度。下列分析正确的是
已知:5I-+IO3-+6H+=3H2O+3I2 I-+3Br2(过量)+3H2O=6H++6Br-+IO3-
方法一I-(样品) IO3-
IO3-
 I2
I2 I-
I-
方法二I-(样品) I2
I2 I-
I-
| A.方法二对样品所做处理操作简便,用作微量的测定更准确 |
| B.当待测液由无色变为蓝色时即达到滴定终点 |
| C.方法一与方法二测量出的样品浓度比为6:l |
| D.假设各步骤操作均得当,方法一所消耗Na2S2O3标准溶液的体积是方法二的6倍 |
下列各类物质中,固态时只能形成离子晶体的是()。
| A.非金属氧化物 | B.非金属单质 | C.强酸 | D.强碱 |
最近科学家成功地制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是()。
| A.该物质的化学式为CO4 |
| B.晶体的熔、沸点高,硬度大 |
| C.晶体中C原子数与C—O键数之比为1∶4 |
| D.晶体的空间最小环共由12个原子所构成 |
纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新材料给予了极大的关注。纳米粒子是指直径为1~100 nm的超细粒子(1 nm=10-9 m)。由于表面效应和体积效应,其常有奇特的光、电、磁、热等性能,可开发为新型功能材料,有关纳米粒子的叙述不正确的是()。
| A.因纳米粒子半径太小,故不能将其制成胶体 |
| B.一定条件下纳米粒子可催化水的分解 |
| C.一定条件下,纳米陶瓷可发生任意弯曲,可塑性好 |
| D.纳米粒子半径小,表面活性高 |
在纳米级的空间中,水的结冰温度是怎样的呢?为此,科学家对不同直径碳纳米管中水的结冰温度进行分析。下图是四种不同直径碳纳米管中的冰柱结构及结冰温度,冰柱的大小取决于碳纳米管的直径。水在碳纳米管中结冰的规律是_________________________。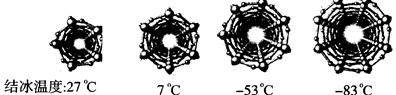
电子表、电子计算器、电脑显示器都运用了液晶材料显示图像和文字。有关其显示原理的叙述中,正确的是()。
| A.施加电场时,液晶分子沿垂直于电场方向排列 |
| B.移去电场后,液晶分子恢复到原来状态 |
| C.施加电场后,液晶分子恢复到原来状态 |
| D.移去电场后,液晶分子沿电场方向排列 |