现有浓度均为0.10mol·L-1的醋酸V1 mL和氢氧化钠溶液V2 mL,下列说法正确的是
| A.常温下,上述溶液中,醋酸溶液的pH=1,氢氧化钠溶液的pH=13 |
| B.常温下,若两溶液混合后pH=7,则混合液:c(Na+)=c(CH3COO-) |
| C.若 V1= V2,将两溶液混合,所得混合液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.V1与V2任意比混合,所得混合液:c (Na+)+ c(H+) =c(OH-)+ c (CH3COO-) |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.0.1L2mol·L-1的(NH4)2S溶液中含有的S2-数目为0.2NA |
| B.7.8g苯中含有C=C键数目为0.3NA |
| C.常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA |
| D.用惰性电极电解1L浓度均为2mol·L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| B.遇苯酚显紫色的溶液:I-、K+、SCN-、Mg2+ |
| C.与铝反应产生大量氢气的溶液:NH4+、Na+、CO32-、NO3- |
| D.加入NaOH后加热既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、CH3COO- |
下列表示物质结构的化学用语或模型正确的是
| A.葡萄糖的最简式(实验式):CH2O |
B.H2O2的电子式: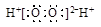 |
C.醛基的电子式: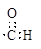 |
D.对-硝基甲苯的结构简式: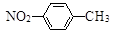 |
在全球气候变暖的背景下,以低能耗、低污染为基础的“低碳经济”成为发展趋向。下列不属于“促进低碳经济”宗旨的是
| A.提高能源效率、寻找替代能源、保护森林以及生态友好型消费 |
| B.推广以液化石油气代替天然气作民用燃料 |
| C.推广利用二氧化碳与环氧丙烷和琥珀酸酐的三元共聚物的生物降解材料 |
| D.推广“绿色自由”计划,吸收空气中CO2并利用廉价能源合成汽油 |
球墨铸铁中含有一种铁碳化合物X。实验室测定化台物X的组成实验如下:
下列说法不正确的是
| A.固体2是Fe2O3 |
| B.溶液甲中可能含有Fe3+ |
| C.X的化学式可以表示为Fe3C2 |
| D.X与足量的热浓硝酸反应有NO2和CO2生成 |