醋酸和盐酸是中学化学中常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=____________(列式,不必化简);下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是______。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________V(醋酸),反应的最初速率为:v(盐酸)_________v(醋酸)。(填写“>”、“<”或“=”)
(3)某同学用0.1000mol/LNaOH溶液分别滴定20.00mL 0.1000mol/LHCl和20.00mL0.1000mol/L CH3COOH,得到如图所示两条滴定曲线,请完成有关问题:
①NaOH溶液滴定CH3COOH溶液的曲线是 (填“图1”或“图2”);
②a= mL。
(4)常温下,将0.1 mol/L盐酸和0.1 mol/L醋酸钠溶液混合,所得溶液为中性,则混合溶液中各离子的浓度按由大到小排序为_______________________________。
(5)已知:90℃时,水的离子积常数为Kw = 3.80×10-13,在此温度下,将pH=3的盐酸和
pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=____________(保留三位有效数字)mol/L。
I.碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应: W(g)+ I2(g) WI2(g)
WI2(g)
为模拟上述反应,在实验室中准确称取0.508 g 碘、0.736 g金属钨放置于50.0mL密闭容器中,并加热使其反应。下图一是混合气体中的WI2蒸气的物质的量随时间变化关系的图像[n(WI2) ~ t]
其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
请回答下列问题:
(1)该反应是(填写“放热”“吸热”)反应。
(2)反应从开始到t1(t1=" 3" min)时间内的平均速率υ(I2)=mol/(L.min)。
(3)在450℃时,计算该反应的平衡常数K=。
(4)能够说明上述反应已经达到平衡状态的有。
| A.I2与WI2的浓度相等 |
| B.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等 |
| C.容器内混合气体的密度不再增加 |
| D.容器内气体压强不变化 |
Ⅱ.图中甲为甲醇燃料电池(电解质溶液为KOH溶液),该同学想在乙中实现铁上镀铜,则a处电极上发生的电极反应式是。
Ⅲ.已知:H2(g)、CO(g)和CH3CH2OH(l)的燃烧热分别为285.8 kJ·mol-1、283.0 kJ·mol-1和1365.5 kJ·mol-1。反应 2CO(g)+4H2(g) CH3CH2OH(l)+H2O(l) 的△H=。
CH3CH2OH(l)+H2O(l) 的△H=。
某强酸性溶液X中含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下: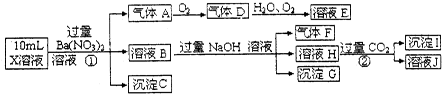
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还一定含有的离子是___________________,有一种阳离子不能确定其是否存在,若要用实验证明该离子一定不存在,其最合理的化学方法是________________。
(2)写出下列反应的离子方程式:
①中生成气体A:___________________。②生成沉淀I:______________________。
(3)假设测定A、F、I均为0.01mol,10mLX溶液中n(H+)=0.04mol,且不能确定含有的离子只有一种。当X溶液中不能确定的离子是_______时,沉淀C物质的量_______。
黄铜矿(CuFeS2)是制铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是(填代号)。
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3
d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。
试用离子方程式表示Fe3+对上述反应的催化过程。、(不必配平)。
(4)利用黄铜矿冶炼铜产生的炉渣(Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液碘水
所选试剂为。证明炉渣中含有的实验现象为。
(共13分)从固体混合物A出发可以发生如下框图所示的一系列变化:

(1)在实验室中常用反应①制取气体C。若要收集气体C,可选择下图装置中的(填字母)
(2)操作②的名称是,在操作②中所使用的玻璃仪器的名称是。
(3)写出下列反应的方程式:反应①的化学方程式
反应③的化学方程式
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过下图中的装置,
其中瓶I中盛放的是,瓶II中盛放的是。
(5)实验中必须吸收多余的气体,以免污染空气。下图是实验室NaOH溶液吸收气体F的装置,为防止发生倒吸现象,合理的装置是(填选项字母)
(共10分)向200 mL ,某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7。
(1)此时溶液的溶质如果是单一成分,可能是____________________;如果是多种成分,可能是__________________________。
(2)在上述所得溶液中,逐滴缓慢滴加2 mol·L-1的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示:
①加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式_______________________。
②B点时,反应所得溶液中溶质的物质的量浓度是__________(溶液体积的变化忽略不计)。