下列有关化学反应速率及限度的描述错误的是
| A.化学反应速率指的是平均速率 |
| B.当化学反应达到其最大限度时,参加反应的物质的质量保持恒定 |
| C.对于同一化学反应,选用不同的物质表示化学反应速率时,其数值一定不同 |
| D.可逆反应不能进行到底,体系中反应物与生成物共存 |
下列反应既属于氧化还原反应,又是吸热反应的是
| A.钠与冷水的反应 | B.甲烷在氧气中的燃烧反应 |
| C.灼热的木炭与CO2反应 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
化学在可持续发展模式中正发挥着积极的作用。下列做法与可持续发展宗旨相违背的是
| A.推广碳捕集和存储技术,逐步实现二氧化碳零排放 |
| B.对工业废水、生活污水净化处理,减少污染物的排放 |
| C.加大铅蓄电池、含汞锌锰干电池的生产,满足消费需求 |
| D.加大清洁能源的开发利用,提高资源的利用率 |
如图所示,某工厂采用电解法处理含铬(Cr2O72﹣)酸性废水,其中,耐酸电解槽以铁板作阴、阳极,电解后,溶液中的Cr2O72﹣全部变为Cr3+,下列说法不正确的是
| A.M与电源的正极相连 | B.出液口排出的溶液中还含有Fe3+ |
| C.N极电极反应为2H++2e﹣==H2↑ | D.阴极区附近溶液pH降低 |
利用下列有关实验装置进行相应的实验,能达到实验目的的是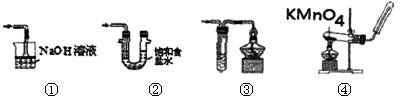
| A.用①装置吸收二氧化硫气体 |
| B.用②装置除去氯气中的氯化氢杂质 |
| C.用③装置可以对硫化氢气体进行尾气处理 |
| D.用④装置制备并收集氧气 |