Ⅰ.含氮化合物西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。已知其相关性质如下表所示:
| 分子式 |
结构简式 |
外观 |
熔点 |
溶解性 |
| C12H10ClN3O |
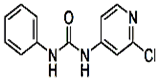 |
白色结晶粉末 |
170~172℃ |
易溶于水 |
(1)氯吡苯脲的晶体类型为_______ ,所含第二周期元素第一电离能从大到小的顺序为
________________(用元素符号表示)。
(2)氯吡苯脲熔点低,易溶于水的原因分别为 _ 。
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。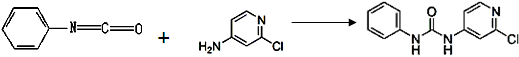
异氰酸苯酯 2-氯-4-氨基吡啶 氯吡苯脲
反应过程中,每生成1mol氯吡苯脲,断裂_______个σ键、断裂_______个π键。
(4)含氮的化合物氨气水溶液逐滴加入硝酸银溶液中制备银氨溶液,写出银氨溶液的配制过程中沉淀溶解的离子方程式 。
Ⅱ.下列是部分金属元素的电离能
| |
X |
Y |
Z |
| 第一电离能(kJ/mol) |
520.2 |
495.8 |
418.8 |
(5)已知X、Y、Z的价层电子构型为ns1,则三种金属的氯化物(RCl)的熔点由低到高的顺序为:
。
(6)RCl可用作有机合成催化剂, 并用于颜料, 防腐等工业。R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如下图所示。元素R基态原子的电子排布式 _ ,
与同一个Cl-相连的 R+有 个。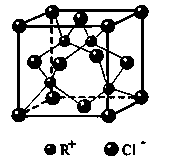
(10分)短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素在周期表中的位置是。
(2)组成单质B的元素的原子结构示意图为。
(3)G与氯酸钠在酸性条件下反应可生成消霉杀菌剂二氧化氯.该反应的氧化剂
为。
(4)溶液F在空气中长期放置生成H的化学反应万程式为:
。
(5)H的溶液与稀硫酸反应产生的现象为
 。
。
(12分)2010年8月7日,甘肃甘南藏族自治州舟曲县发生大泥石流,造成大量人员伤亡,其中饮用水安全在灾后重建中占有极为重要的地位,某研究小组提取三处被污染的水源进行分析,并给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处 含有E物质,A、B、C、D、E五种常见化合物都是由下表中的离子形成的:
含有E物质,A、B、C、D、E五种常见化合物都是由下表中的离子形成的:
| 阳离子 |
 |
| 阴离子 |
 |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液。
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解。
③进行焰色反应实验,只有B、C含有钾离子。
④在各溶液中加入 溶液,再加入过量稀硝酸,A中放出无色气体,C、D
溶液,再加入过量稀硝酸,A中放出无色气体,C、D
中产生白色沉淀。
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上 述实验现象
述实验现象 填写下列空白:
填写下列空白:
(1)写出B、C、D的化学式:B、C、D.
(2)将含lmolA的溶液与含lmolE的溶液反应后蒸干,仅得到一种化合物,该化合物为。
(3)写出实验②发生反应的离子方程式
.
(4)C常用作净水剂,用离子方程式表示其净水原理
。
(14分)某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去。提供的试剂:研细的钙片粉末 (钙片中的其他成分不与 盐酸反应)、
盐酸反应)、 盐酸、5%NaOH溶液、饱和
盐酸、5%NaOH溶液、饱和 溶液、饱和
溶液、饱和 溶液和蒸馏水。
溶液和蒸馏水。
实验过程:
Ⅰ.检查两套装置的气密性。
Ⅱ.在A、C的右边加入0.25g钙片粉末,左边加入3mL 盐酸,塞紧塞子。在B、E中均加入饱和
盐酸,塞紧塞子。在B、E中均加入饱和 溶液,如图所示,记下量气管读数。
溶液,如图所示,记下量气管读数。
Ⅲ.将A、C倾斜,使液体与固体混合,实验结束并冷却后读出量气管读数,测得B中收集到的气体为41.90mL,E中收集到的气体体积为39.20mL(以上气体体积均已折算为标准状况下的体积)。
回答下列问题:
(1)Ⅰ中检查图1装置气密性的方法是
。
(2)A中发生反应的离子方程式为;
D中加入试剂为,D的作用是。
(3)实验前左右两管液 面在同一水平面上,最后读数时右管的液面高于左管的液面,应进行的操作是
面在同一水平面上,最后读数时右管的液面高于左管的液面,应进行的操作是 。
。
(4)图2实验所得钙片中的碳酸钙的质量分数为;图1实验比图 2实验所得钙片中的碳酸钙含量偏高,用离子万程式表示偏高的原因
。
(10分)实验是化学研究的重要手段,贯穿于化学学习的始终。试回答下列中学化学实验室中常见仪器的有关问题:
(1)在仪器①分液漏斗②试剂瓶③集气瓶④滴定管⑤容量瓶⑥量筒⑦托盘天平中,标有"0"刻度的是(填序号,下同) ;标有使用温度的仪器是。
(2)"磨砂"是增加玻璃仪器密封性的一种处理工艺。在仪器①试管②分液漏斗
③细口试剂瓶④广口试剂瓶⑤集气瓶⑥酸式滴定管⑦碱式滴定管中,用到"磨砂"的有
 。
。
(3)在仪器①漏斗②容量瓶③蒸馏烧瓶④分液漏斗⑤烧杯⑥蒸发皿 中,可用于粗盐提纯实验的有;可用于分离两种沸点接近且互不相溶的液态混合物 (即分液)实验的有。
(16分,每空2分)某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据 下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、
下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、 NaOH溶液等试剂)
NaOH溶液等试剂)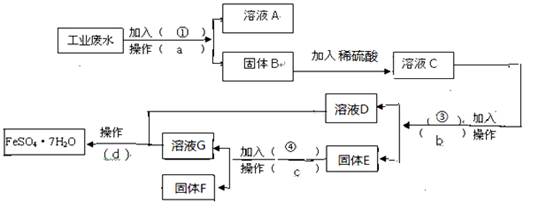 (1)操作a的名称为,所需要的玻璃仪器为____。
(1)操作a的名称为,所需要的玻璃仪器为____。
(2)固体E的成分为 ____,加入的试剂④为__,发生的化学方程式为。
____,加入的试剂④为__,发生的化学方程式为。
(3)加入试剂①的目 的是____________。
的是____________。
(4)从溶液D和溶液G中得到FeSO4.7H2O晶体的操作为、冷却结晶 、
、洗涤、干燥。