关于金属物理性质原因的描述不正确的是
| A.金属具有良好的导电性,是因为金属晶体中的“电子气”在电场作用下作定向移动 |
| B.金属具有良好的导热性能,是因为自由电子受热后运动速率增大,与金属离子碰撞频率增大,传递了能量 |
| C.金属晶体具有良好的延展性,是因为金属晶体中的原子层在滑动过程中金属键未破坏 |
| D.金属一般具有银白色光泽,是物理性质,与金属键没有关系 |
设NA为阿伏加德罗常数的值。下列说法正确是
| A.标准状况下,2.24 L三氯甲烷中含有碳氯共价健的数目为0.3NA |
| B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| C.常温常压下,28 g C2H4、C3H6的混合气体中含有碳原子的数目为2NA |
| D.0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA |
用下列实验装置进行相应的实验,能达到实验目的的是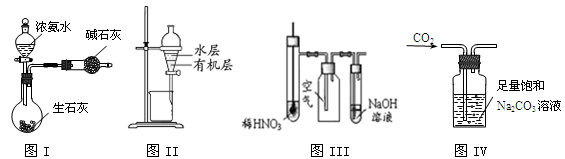
| A.图I所示装置制取干燥的氨气 |
| B.图II所示装置用于提取I2的CCl4溶液中的I2 |
| C.图III所示装置微热稀HNO3,在广口瓶中可收集NO气体 |
| D.图IV所示装置可用于除去CO2中含有的少量HCl |
下列有关物质性质、应用的说法正确的是
| A.氯化铝是电解质,可电解其水溶液获得金属铝 |
| B.二氧化硅具有导电性,可用于生产光导纤维 |
| C.SO2具有漂白性,可用于将银耳漂白为“雪耳” |
| D.小苏打可与酸反应,可用作治疗胃酸过多的药剂 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.c(ClO-)=1.0mol·L-1的溶液中:Na+、SO32-、S2-、SO42- |
| B.由水电离的c(H+)=1×10-12 mol·L-1的溶液中:Ba2+、K+、Cl-、NO3- |
| C.常温下,c(H+)/c(OH-)=10-10的溶液中:Ca2+、Mg2+、HCO3-、I- |
| D.滴入少量KSCN溶液显红色的溶液中:Na+、K+、I-、SO42- |
下列有关化学用语表示正确的是
| A.明矾的化学式:KAl(SO4)2 |
B.氯离子的结构示意图: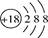 |
C.中子数为10的氧原子: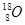 |
D.溴化铵的电子式: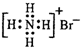 |