山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为
CH3—CH=CH—CH=CH—COOH。下列关于山梨酸的叙述不正确的是
| A.山梨酸易溶于四氯化碳 |
| B.山梨酸能与氢气发生加成反应 |
| C.山梨酸能和乙醇反应生成酯 |
| D.1 mol山梨酸能和金属钠反应生成1 mol氢气 |
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,
下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-= 4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是
| A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 |
| B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 |
| C.电镀工业中,X是待镀金属,Y是镀层金属 |
| D.外加电流的阴极保护法中,Y是待保护金属 |
如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)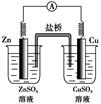
| A.反应中,盐桥中的K+会移向CuSO4溶液 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.铜片上有气泡逸出 |
| D.反应前后铜片质量不改变 |
一定温度下,反应N2(g)+3H2(g)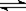 2NH3(g)的反应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g)
2NH3(g)的反应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g) 2N2(g)+6H2(g)的反应热和化学平衡常数为
2N2(g)+6H2(g)的反应热和化学平衡常数为
| A.2△H和2K | B.-2△H和 K2 |
| C.-2△H和 K-2 | D.2△H和-2K |
下列叙述正确的是
| A.工业上电解熔融的Al2O3冶炼铝用铁做阳极 |
| B.用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1∶2 |
| C.用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1molNaOH |
| D.用惰性电极电解CuSO4溶液一段时间后,加入Cu(OH)2固体可以使CuSO4溶液恢复原来浓度 |