沼气(主要成分是甲烷)是一种廉价的能源,把农村中大量存在的农作物秸秆、杂草、人畜粪便等在沼气池中发酵,便可产生沼气,沼气完全燃烧可以用来点灯、做饭。
(1)在101kPa时,32gCH4燃烧生成CO2和气态H2O,放出1604kJ的热量,写出甲烷燃烧的热化学方程式为__________________________________________________________。
(2)120℃,取CH4和过量O2的混合气体共0.4mol,点燃使其充分反应,将燃烧后的气体通过足量的碱石灰(NaOH和CaO的固体混合物)充分吸收,碱石灰增重8g。计算:原混合气体中CH4和O2的体积比是多少?
体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①________②(填“>”、“<”或“=”,下同);与完全相同的镁条发生反应,开始时的反应速率:①______ ②; 中和等量NaOH时消耗的体积:①________②;与足量的Zn反应生成H2的物质的量:① ________②。
中和等量NaOH时消耗的体积:①________②;与足量的Zn反应生成H2的物质的量:① ________②。
某有机物A由C、H、O三种元素组成,90克A完全燃烧可生成132克CO2和54克H2O。试求:
(1)该有机物的最简式。
(2)若符合该最简式的A物质可能不止一种,则它们之间的关系(填序号)
A.一定互为同系物 B.一定互为同分异构体
C.等质量的它们完全燃烧耗氧量相同 D.等物质的量的它们完全燃烧耗氧量相同
(3)若A是具有水果香味的液体,可发生水解反应,写出A与NaOH溶液反应的化学方程式
。
(4)若A的相对分子质量为180,能发生银镜反应,也能发生酯化反应,则A的结构简式为_______________.
A、C、E、H是常见单质,B、F是常见氧化物,D是无色液体,I的焰色反应呈黄色。它们之间的转化关系如图所示:请回答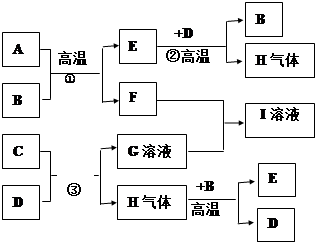
(1) 写出反应式①②的化学方程式:
①,
②。
(2)写出反应③的离子方程式________________。
(3)写出 A和G溶液反应的离子方程式:。
8分)某有机物的结构简式为 HOCH2 CH=CHCOOH,
(1)写出该有机物中所含的官能团的名称________________________________
(2)写出该有机物与溴水反应的化学方程式________________________________
(3)写出该有机物与足量NaHCO3溶液反应的化学方程式_____________________
(4)写出该有机物与乙酸反应的化学方程式________________________________
(9分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010. |
0.008 |
0.007 |
0. 007 |
0.007 |
⑴NO的平衡转化率为_______
⑵下图中表示NO2的浓度变化曲线是。
用O2表示从0~2s内该反应的平均速率v=。
⑶能说明该反应已达到平衡状态的是。
a.v (NO2)="2" v (O2) b.容器内压强保持不变
c.v逆(NO)="2" v正 (O2) d.容器内混合气体的密度保持不变
e.该容器内颜色保持不变