下列叙述不正确的是
A.用电子式表示HCl的形成过程: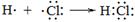 |
B. 中的原子核内的中子数与核外电子数之差是99 中的原子核内的中子数与核外电子数之差是99 |
C.在空气中加热金属锂:4Li+O2 2Li2O 2Li2O |
D.铝热法炼铁:2Al+Fe2O3 2Fe+ Al2O3 2Fe+ Al2O3 |
列关于甲烷结构的说法错误的是
| A.甲烷分子中的化学键都是共价键 | B.甲烷分子为正四面体结构 |
| C.甲烷分子为正四边形结构 | D.CH2C12不存在同分异构体 |
2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR'。则分子式为C4H8的烯烃中,任取两种发生“复分解反应”,生成新烯烃种类最多的一种组合中,其新烯烃的种类为
| A.5种 | B.4种 | C.3 种 | D.2种 |
1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子。如下图分子,因其形状像东方塔式庙宇(pagoda—style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是
| A.分子式为C20H20 |
| B.一氯代物的同分异构体只有两种 |
| C.分子中含有二个亚甲基(—CH2—) |
| D.分子中含有4个五元碳环 |
下列说法正确的是()
| A.某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n |
| B.一种烃在足量的氧气中燃烧并通过浓H2SO4,减少的体积就是生成的水蒸气的体积 |
| C.某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4;若体积减少,则y>4;否则y<4 |
| D.相同质量的烃,完全燃烧,消耗O2越多,烃中含H%越高 |
重结晶过程中如果溶剂对杂质的溶解很少,对有机物的溶解性比较强,那么趁热过滤后()
| A.有机物仍然在滤液中 | B.杂质在滤液中 |
| C.有机物停留在滤纸上 | D.杂质停留在滤纸上 |