已知:①一个碳原子上连有两个羟基时,易发生下列转化:(R、R'代表烃基或氢原子)。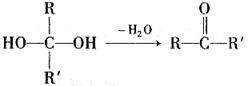
②同一个碳原子上连有两个双键的结构不稳定。根据下图回答有关问题: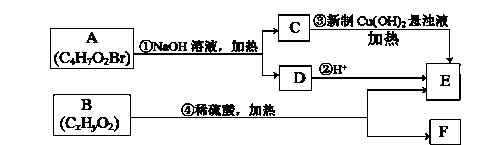
(1)E中含有的官能团的名称是 ;C与新制氢氧化铜反应的化学方程式为 。
(2)A的结构简式为 。A不能发生的反应有 (填字母)。
a.取代反应 b.消去反应 c.酯化反应 d.还原反应
(3)已知B的相对分子质量为188,其充分燃烧的产物中n(CO2):n(H2O)=2:1。则B的分子式为 。
(4)F具有如下特点:①能与FeCl3溶液发生显色反应;②核磁共振氢谱中显示有五种吸收峰;③苯环上的一氯代物只有两种;④除苯环外,不含有其他环状结构。写出两种符合上述条件,具有稳定结构的F可能的结构简式: 。
(1) 在带有活塞的密闭容器中发生反应:Fe2O3+3H2===2Fe+3H2O,采取下列措施不能改变反应速率的是( )
| A.增大Fe2O3的投入量 |
| B.保持容器的体积不变,增加H2的输入量 |
| C.充入N2,保持容器内压强不变 |
| D.充入N2,保持容器体积不变 |
往容积为10 L的密闭容器内通入40 mol N2和120 mol H2,在一定条件下进行反应,经2 s后达到平衡状态,平衡时c(N2)为2 mol/L。
(2)用H2的浓度变化表示2 s内的平均速率v(H2)=________。
(3)氮气的转化率是________。
(4)平衡时混合气体中氨的体积分数是________。
(5)容器内反应前后压强比是________。
原电池中发生的化学反应属于,原电池将转化为能。其中,电子流出的一极是原电池的极,该极发生反应,电子流入的一极是原电池的极,该极发生反应。原电池中电解质溶液的作用是。
下列反应中,属于吸热反应的是。
①煅烧石灰石(主要成分是CaCO3)制生石灰(CaO)②燃烧木炭取暖③炸药爆炸 ④ 酸与碱的中和反应 ⑤ 生石灰与水作用制熟石灰 ⑥ 食物因氧化而腐败
从能量的角度看,断开化学键要,形成化学键要。一个化学反应是释放能量还是吸收能量取决于。
写出下列物质的电子式:①KCl;②Cl2;③H2O。