下列依据相关实验得出的结论正确的是
| A.向FeCl2溶液中滴加少量KSCN溶液变血红色,说明FeCl2完全被氧化成FeCl3 |
| B.向某溶液中加入稀硝酸再滴入Ba(NO3)2溶液产生白色沉淀,该溶液一定含SO42- |
| C.向漂白粉上加入较浓的盐酸,产生的气体不能使湿润淀粉碘化钾试纸变蓝,说明该漂白粉已经失效 |
| D.向浓度均为0. 1 mol·L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液,产生黄色沉淀,说明Ksp(AgCl)<Ksp(AgI) |
用相对分子质量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃的数目为()
| A.3 | B.4 | C.5 | D.6 |
下列哪个选项属于碳链异构()
| A.CH3CH2CH2CH2CH3和CH3CH(CH3)2 |
| B.CH2=C(CH3)2和CH3CH2CH=CH2 |
| C.CH3CH2OH和CH3OCH3 |
| D.CH3CH2CH2COOH和CH3COOCH2CH2 |
下列实验要用到温度计的是()
| A.乙酸乙酯的制备 | B.对8%的乙醇水溶液进行蒸馏 |
| C.对粗苯甲酸进行重结晶 | D.铜片与浓硫酸加热反应 |
在C2H2、C6H6、C2H4O组成的混合物中,已知氧元素的质量分数为8%,则混合物中碳元素的质量分数是()
| A.92.3% | B.87.6% | C.75% | D.84% |
某烃在光照条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是()
A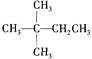 B CH3CH2CH2CH3 C
B CH3CH2CH2CH3 C D CH3-
D CH3- -CH3
-CH3