常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液: c(NH4+)>c(SO42-)>c(Fe2+)>c(H+) |
| B.0.1 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C.0.1 mol·L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO32-) |
| D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是
A B C D
下列叙述正确的是
| A.将5.85 g NaCl晶体溶入100 mL水中,制得0.10 mol/L的NaCl溶液 |
| B.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol/L |
C.将w g a%的NaCl溶液蒸发掉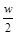 g水,可得到2a%的NaCl溶液( g水,可得到2a%的NaCl溶液( >2a%) >2a%) |
| D.将1体积c1mol/L的硫酸用水稀释为5体积,所得稀溶液的浓度为0.2c1mol/L |
下列说法正确的是
A.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O中,氧化剂和还原剂物质的量之比为1∶2 MnCl2+Cl2↑+2H2O中,氧化剂和还原剂物质的量之比为1∶2 |
| B.2H2S+SO2=3S↓+2H2O中,氧化产物和还原产物物质的量之比为1∶1 |
C.3S+6KOH  2K2S+K2SO3+3H2O中,被氧化和被还原的硫元素质量之比为2∶1 2K2S+K2SO3+3H2O中,被氧化和被还原的硫元素质量之比为2∶1 |
| D.5NH4NO3=4N2+2HNO3+9H2O中,反应中发生氧化反应和发生还原反应的氮元素质量之比为5∶3 |
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:
2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O
2ClO2↑+K2SO4+2CO2↑+2H2O
下列说法中错误的是
| A.KClO3在反应中得到电子 |
| B.ClO2是还原产物 |
| C.H2C2O4在反应中被氧化 |
| D.1 mol KClO3参加反应,有2 mol电子转移 |
设NA代表阿伏加德罗常数,下列说法正确的是
| A.标准状况下11.2 L O2和16 g O3中含有的氧原子数均NA |
| B.5.6 g金属铁变成亚铁离子时失去的电子数目的0.2NA |
| C.2.24 L CO与N2混合气体中所含电子数目为1.4NA |
| D.1 mol·L-1的CaCl2溶液中含有的Cl—为2NA |