氢能源是一种重要的清洁能源。现有两种可产生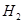 的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 L的
的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 L的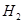 (已折算成标准状况)。甲与水反应也能产生
(已折算成标准状况)。甲与水反应也能产生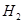 ,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到
,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到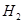 和另一种单质气体丙,丙在标准状态下的密度为1.25g·L-1。请回答下列问题:
和另一种单质气体丙,丙在标准状态下的密度为1.25g·L-1。请回答下列问题:
(1)甲的化学式是_________;乙的空间构型是__________。
(2)甲与水反应的化学方程式是__________________________________。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式________ 有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之
_________________________。
(已知Cu2O+2H+==Cu+Cu2++H2O)
(5)甲与乙之间_______(填“可能”或“不可能)发生反应产生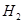 ,判断理由是
,判断理由是
_______ _ 。
(5分)二氧化硅晶体中,每个硅原子周围有个氧原子,每个氧原子周围有个硅原子,硅氧原子个数比为。若去掉二氧化硅晶体中的氧原子,且把硅原子看作碳原子,则所得到空间网状结构与金刚石空间网状结构相同,试推测每个硅原子与它周围的4个硅原子所形成的空间结构为型;并推算二氧化硅晶体中最小的硅氧原子环上共有个原子
下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
(1)单质B的化学式是,单质F的化学式是________ ,写出物质A的一种用途。
(2)写出单质B与强碱溶液反应的离子方程式,写出由沉淀J生成 H溶液的离子方程式,
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式,白色沉淀L会迅速变为色,最终变为红褐色沉淀G,写出L变为G的化学反应方程式。
(4)溶液I中所含金属离子是_____________________。
实验室盛放氢氧化钠溶液的试剂瓶不用玻璃塞,是因为玻璃中含有(填化学式),刻蚀玻璃常用的试剂是(填化学式),发生反应的化学方程式为,传统陶瓷的主要成分是类物质。
金属钠在实验室通常保存在中,切下一小块钠进行化学实验,要用到的实验用品有,金属钠失火时,应该用灭火。过氧化钠与水反应,(填化学式)作还原剂,反应后的溶液中加入酚酞的现象是。
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示:
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为、;
(2)闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是,电解氯化钠溶液的化学方程式为;
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上通过电解池的电量为
(已知NA=6.02×1023mol-1,电子电荷为1.60×10-19C,列式表示即可),最多能产生的氯气体积为L(标准状况)。