已知33As、34Se、35Br位于同一周期,下列关系正确的是
| A.电负性:As>Cl>P | B.热稳定性:HCl>HBr>AsH3 |
| C.第一电离能:Br>Se>As | D.酸性:H3AsO4>H2SO4>H3PO4 |
在下列溶液中,各组离子一定能够大量共存的是()
D.在由水电离出的 的溶液中:
的溶液中: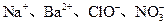
B.能使广泛pH试纸显蓝紫色的溶液:K+、Ba2+、Cl—、Br—
C.常温下c(H+)/c(OH-)=1012的溶液:Fe2+、Mg2+、NO3—、Cl—
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32-
室温下,一元酸HA溶液与一元碱BOH溶液等体积混合,下列有关判断正确的是
| A.若混合后所得溶液呈中性,则HA肯定是强酸、BOH肯定是强碱 |
| B.若混合前酸、碱pH之和等于14,混合后所得溶液呈碱性,则BOH肯定是弱碱 |
| C.若混合前酸、碱物质的量浓度相同,混合后所得溶液呈酸性,则HA肯定是弱酸 |
| D.若混合后所得溶液呈酸性,则混合溶液中离子浓度一定满足 |
c(B+ )>c(A-)>c(H+)>c(OH-)
)>c(A-)>c(H+)>c(OH-)
下列说法中不正确的有()
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂;②光照氯水有气泡逸出,该气体是Cl2; ③燃煤时加入适量石灰石,可减少废气中SO2的量;④pH在5.6~7.0之间的降水通常称为酸雨;⑤室温下浓硫酸与铜片不会发生剧烈的化学反应,原因是铜被钝化。⑥氯气易液化,液氯可以保存在钢瓶中;⑦常温下浓硫酸可以用铝制容器盛放;⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤
| A.2个 | B.3个 | C.4个 | D.5个 |
下列离子方程式书写正确的是()
| A.过量的SO2通人NaOH溶液中:SO2+2OH-=SO32-+H2O |
B.Fe(NO3)3溶液中加入过量的HI溶 液:2Fe3++2I-=2Fe2++I2 液:2Fe3++2I-=2Fe2++I2 |
| C.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2—+6H+=2Mn2++5NO3-+3H2O |
| D.NaHCO3溶液中加入过量的Ba(OH)2溶液: |
2HCO32-+Ba2++2OH-=BaCO3↓+2H2O+CO32
下列实验室除杂(括号内为少量杂质)的方案正确的是()
| 提纯物质 |
除杂试剂 |
提纯方法 |
|
| A |
苯(苯酚) |
碳酸钠溶液 |
过滤 |
| B |
Al(Fe) |
氢氧化钠溶液 |
过滤 |
| C |
CO2(NO2) |
水 |
洗气 |
| D |
乙酸乙酯(乙醇) |
水 |
水洗、分液 |