学校附近的湖水中浮萍疯长,助长水质恶化。湖水水样中可能含有Fe3+、Ba2+、K+、H+、NO3-、Cl-、CO32-、SO42-离子。为了进一步确认,取样进行实验检测:
①取水样仔细观察,呈透明、均一状态。
②用pH试纸测定污水的pH,试纸显红色。
③向水样中滴入KSCN溶液,呈红色。
④向水样中滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失。
(1)由此可知,该污水中肯定含有的离子是_________,肯定没有的离子是_________。
(2) 浮萍疯长的可能原因是水中含有较多的_____________离子。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍;A的一种原子中,质量数与质子数之差为零。D元素的原子最外层电子数为m,次外层电子数为n;E元素的原子L层电子数为m+n,M层电子数为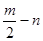 。请回答下列问题:
。请回答下列问题:
(1)B元素是____________,D元素在周期表中的位置是_____________________;
(2)C与E形成的化合物E3C属于________晶体(填“原子”、“离子”或“分子”);
(3)由A、D、E元素组成的化合物中存在的作用力是_________________________;
(4)写出一个E和D形成的化合物与水反应的离子方程式_______________________;
(5)已知:甲 + H2O → 丙 + 丁。若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,丙具有漂白性。则甲中Cl元素的化合价是 ,丁与H2O有相同的电子总数,则丁的电子式为。 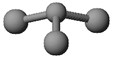
(6)与D同主族上下相邻的元素M、N,原子电子层数M>N>D,三种元素氢化物沸点由大到小的顺序是(填写化学式)。
有机物A~E的转化关系如下所示。1molA能与1molBr2恰好完全反应;E的分子式为C5H10O3, 1molE分别与Na、NaHCO3反应,消耗两者物质的量之比为2∶1,氢核磁共振谱分析E有5组不同的特征峰。F分子结构中含有一个六元环。已知: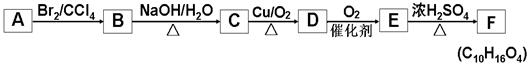
(1)E中含有的官能团名称是,E的结构简式是
(2)写出C→D的化学方程式,反应类型______
(3)写出E→F的化学方程式,反应类型______
(4)E转化为F过程中,可能发生多种副反应,写出含5个碳原子的副产物的键线式
____________________、______________________
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+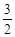 O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下:
O2(g) ="=" CO2(g)+2H2O(l)。其工作原理示意图如下: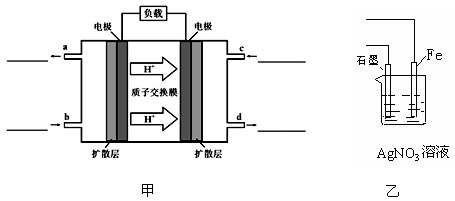
请回答下列问题:
(1)写出甲图中b、c两个入口通入的物质名称(或化学式)bc
(2)负极的电极反应式为
(3)用该原电池电解AgNO3溶液,若Fe电极增重5.4g,则燃料电池在理论上消耗的氧气的体积为mL(标准状况)
某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是:和。
(2)试通过计算确定该结晶水合物的化学式为。
(3)①加入Ba(OH)2溶液后,若所得沉淀的总物质的量最大,则反应的离子方程式为
。
②若加人75mL的Ba(OH)2溶液,则得到的沉淀质量为g。
有下列七种溶液:
| A.氢氧化钠溶液; | B.氢氧化钡溶液; | C.硫酸铝溶液; | D.明矾溶液; |
E、混有少量硝酸的硫酸镁溶液;F、氯化铁溶液;
任取其中的一种溶液(甲)逐滴加入到另一种溶液(乙)中至过量,观察到自始至终均有白色沉淀。试回答下列问题:
(1)产生上述实验现象的试剂组合有(请用字母代号逐一列出,表格各栏可填满,可不填满,也可补充)
| 组别 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
| 甲 |
B |
|||||||
| 乙 |
D |
(2)请在下列坐标中作出第1组实验所得沉淀的物质的量(n沉淀/mol)随B溶液体积(VB/L)变化的曲线。
(3)下图是某一组实验中所得沉淀的物质的量(n沉淀/mol)随甲溶液中溶质的物质的量(n甲/mol)变化的曲线。符合下图曲线的试剂组合是:甲(填化学式);乙(填化学式)。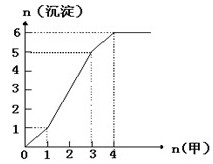
若实验时取用的乙溶液为500 mL,试计算乙溶液中溶质的物质的量的浓度