设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 molCl2与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,2.24 L NH3中含有共价键的数目为NA |
| C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| D.标况下,11.2 L SO3所含的分子数目为0.5NA |
下列有关生活中常见有机物的说法正确的是( )
| A.甲烷和氯气光照条件下发生取代反应,产物是气体与液体的混合物 |
| B.液化石油气和天然气的主要成分都是甲烷 |
| C.苯和乙烯都能使溴水层变为无色,二者都是发生加成反应 |
| D.煤干馏可得煤油,甲烷、乙烯和苯都能从石油中分馏得到 |
下列化合物的分子中,所有原子都处于同一平面的是( )
| A.乙烷 | B.甲苯 | C.氟苯 | D.氯乙烷 |
下列反应中,属于取代反应的是( )
①CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |
对下列化学用语的理解正确的是( )
A.离子结构示意图 既可以表示35Cl-,也可以表示37Cl- 既可以表示35Cl-,也可以表示37Cl- |
B.电子式 既可以表示羟基,也可以表示氢氧根离子 既可以表示羟基,也可以表示氢氧根离子 |
C.比例模型 既可以表示甲烷分子,也可以表示四氯化碳分子 既可以表示甲烷分子,也可以表示四氯化碳分子 |
| D.结构简式(CH3)2CHCH3既可以表示正丁烷,也可以表示异丁烷 |
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。下列判断正确的是( )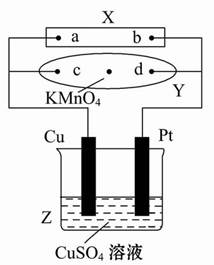
| A.滤纸上c点附近会变红色 |
| B.Cu电极质量减小,Pt电极质量增大 |
| C.Z中溶液的pH先减小,后增大 |
| D.溶液中的SO42-向Cu电极定向移动 |