一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g) + Y(g) 2Z(g) + M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g) + M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
| A.用X表示5min内此反应的反应速率是(0.1—0.2a)mol·(L·min)—1 |
| B.当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
| C.向平衡后的体系中加入l mol M,平衡向逆反应方向移动 |
| D.向上述平衡体系中再充入l mol X,v(正)增大,v(逆)减小,平衡正向移动 |
对于化学反应能否自发进行,下列说法中错误的是 ( )
| A.若ΔH<0,ΔS>0,任何温度下都能自发进行 |
| B.若ΔH>0,ΔS<0,任何温度下都不能自发进行 |
| C.若ΔH>0,ΔS>0,低温时可自发进行 |
| D.若ΔH<0,ΔS<0,低温时可自发进行 |
某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g) 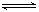 cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是()
cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是()
| A.平衡正移 | B.(a+b)>(c+d) |
| C.Z的体积分数变小 | D.X的转化率变大 |
在某温度下,H2和I2各0.10mol的气态混合物充入10L的密闭容器中,发生反应:H2(g)+I2(g) 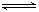 2HI(g),充分反应后达到平衡,测得c(H2)="0.008" mol•L-1,则该反应的平衡常数为( )
2HI(g),充分反应后达到平衡,测得c(H2)="0.008" mol•L-1,则该反应的平衡常数为( )
| A.40 | B.62.5 | C.0.25 | D.4 |
在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g)  2C(g),可以判断达到化学平衡状态的是( )
2C(g),可以判断达到化学平衡状态的是( )
| A.体系压强不变 | B.单位时间消耗n molA,同时生成2nmolC |
| C.A的转化率不变 | D.容器内气体密度不变 |
某温度下,H2(g)+CO2(g)  H2O(g)+CO(g)的平衡常数K=9/4.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示.
H2O(g)+CO(g)的平衡常数K=9/4.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示.
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)(mol/L) |
0.010 |
0.020 |
0.020 |
| c(CO2)(mol/L) |
0.010 |
0.010 |
0.020 |
下列判断不正确的是()
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中CO2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢