下图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是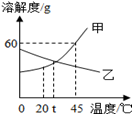
| A.t℃时,甲、乙两物质的溶解度相等 |
| B.甲物质的溶解度为60g |
| C.升高温度可使不饱和的甲溶液变为饱和 |
| D.乙物质的溶解度随温度的升高而增大 |
决定元素种类的是原子的()
| A.质子数 | B.中子数 | C.电子数 | D.最外层电子数 |
空气的成分中,体积分数约占78%的是( )
| A.氧气 | B.氮气 | C.二氧化碳 | D.稀有气体 |
下列生活事例中,主要过程为化学变化的是( )
| A.功夫深,铁杵成针 | B.佳节到,焰火缤纷 |
| C.春天来,冰雪消融 | D.美酒开,满屋飘香 |
从微观视角认识事物是化学的重要特点。对下列现象解释正确的是 ( )
| A.“墙内开花墙外香”是因为分子在不断运动 |
| B.热胀冷缩是因为分子大小随温度变化而改变 |
| C.气体易被压缩是因为气体分子间隔很小 |
| D.蔗糖放在水中后消失是因为蔗糖分子被分解了 |
鉴别空气、氧气和二氧化碳三瓶气体,最常用的方法是( )
| A.分别测定它们的密度 | B.将燃着的木条分别伸入集气瓶中 |
| C.观察颜色并闻它们的气味 | D.将气体分别通入紫色石蕊溶液中 |