能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________(填序号)。
a. Ba(OH)2·8H2O与NH4Cl混合搅拌
b. 高温煅烧石灰石
c. 铝与盐酸反应
②某同学进行如下图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是_______(填“吸热”或“放热”)反应,其离子方程式是_______________。
(2)电能是现代社会应用最广泛的能源之一。
下图所示的原电池装置中,其负极是_____________________,正极上能够观察到的现象是____________________________,正极的电极反应式是_________________________。
原电池工作一段时间后,若消耗锌6.5g,则放出气体__________g。
在某有机物A的分子中,其结构简式如下图。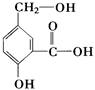
(1)A跟NaOH溶液反应的化学方程式是
(2)A跟NaHCO3溶液反应的化学方程式是
(3)A在一定条件下跟Na反应的化学方程式是:
香草醛结构简式为: ,请按要求完成下列问题:
,请按要求完成下列问题:
(1)香草醛有多种同分异构体,其中苯环上的一溴代物只有两种且属于芳香酸的结构简式___________;
(2)香草醛的同分异构体中属于芳香酯有种。其中某些酯与NaOH作用只能消耗等物质的量的NaOH,写出符合该条件的一种酯在NaOH溶液中水解的化学方程式:。
(3)写出香草醛发生银镜反应的化学方程式:______________________________。
(3分)肉桂醛的结构为: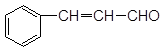
①把足量肉桂醛加入到溴水中,溴水褪色了,这____________(填“能”或“不能”)说明肉桂醛中存在碳碳双键。
②检验分子中碳碳双键的方法是_______________。
(3分)在硫酸铜溶液中加入过量的氢氧化钠溶液后,再滴入足量乙醛溶液,加热。实验过程中发生的反应的化学方程式为。
(l)常温下,如果取0.1mol•L﹣1HA溶液与0.1mol•L﹣1NaOH溶液等体积混合,测得混合液的pH=8.混合液中由水电离出的OH﹣浓度与0.1mol•L﹣1NaOH溶液中由水电离出的OH﹣浓度之比为_________ .
(2)相同温度下,将足量硫酸钡固体分别放入相同体积的①0.1mol•L﹣1硫酸铝溶液 ②0.1mol•L﹣1氯化钡溶液 ③蒸馏水 ④0.1mol•L﹣1硫酸溶液中,Ba2+浓度由大到小的顺序是_________ .(用序号填写)
(3)常温下,将a mol•L﹣1的氨水与0.1mol•L﹣1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl﹣)时,用含a的代数式表示NH3•H2O的电离常数Kb= _________ mol•L﹣1.