某无色溶液中含有K+,Cl-,OH-,SO32-,SO42-,为了检验除OH-外的其它所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氢氧化钡溶液、溴水和酚酞六种试剂,设计如下实验步骤,并记录相关现象: 下列有关结论错误的是 ( )
下列有关结论错误的是 ( )
| A.试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl |
| B.现象3中白色沉淀是BaSO4 |
| C.试剂②是盐酸,试剂③是硝酸 |
| D.产生现象2的离子方程式是:Br2+2H2O+SO2=4H++2Br-+SO42- |
氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可生成CuH。下列叙述中错误的是()
| A.“某物质”具有还原性 |
| B.CuH与盐酸反应可能产生H2 |
| C.CuH与足量稀硝酸反应:CuH+3H++NO3-=Cu2++NO↑+2H2O |
| D.CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl |
海水资源的综合利用十分重要,不需要通过化学变化就能够从海水中获得的物质是( )
| A.食盐、淡水 | B.钠、镁 | C.烧碱、氯气 | D.溴、碘 |
2015年8月12日晚11时许,天津市塘沽开发区一带发生爆炸事故,现场火光冲天。据多位市民反映,事发时十公里范围内均有震感,抬头可见蘑菇云,安全问题再次敲响了警钟。下列关于安全问题的说法,不正确的是()
| A.危险化学品包括:爆炸品、易燃物质、自燃自热物质、氧化性气体、加压气体等 |
| B.金属钠着火不能用水灭火,应使用干砂灭火 |
| C.处置实验过程产生的剧毒药品废液,稀释后用大量水冲净 |
| D.简单辨认有味的化学药品时,将瓶口远离鼻子,用手在瓶口上方扇动,稍闻其味即可 |
室温时,向20 mL 0.1 mol/L醋酸溶液中不断滴入0.1 mol/L NaOH溶液,溶液pH变化曲线如图所示。下列关于溶液中离子浓度大小关系的描述正确的是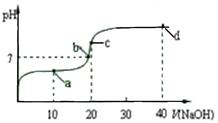
| A.a点时:c(CH3COOH) c(CH3COO-) c(H+) c(Na+) c(OH-) |
| B.b点时:c(Na+) c(CH3COO-) |
| C.c点时:c(H+)=c(CH3COOH)+c(OH-) |
| D.d点时:c(Na+) c(OH-) c(CH3COO-) c(H+) |
以下说法正确的是
①某溶液加入稀盐酸产生无色无味的气体,将气体通入澄清石灰水溶液变浑浊,则溶液中一定含有大量CO32-Na2CO3
②向饱和FeCl3溶液中滴加过量氨水制取Fe(OH)3胶体
③除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:BaCl2溶液→NaOH
溶液→Na2CO3溶液→过滤后加盐酸
④工业上常用铁质容器盛冷浓硫酸,因为浓硫酸有强氧化性,能使铁钝化阻止反应进一步进行
⑤实验室用图1所示装置制备并收集收集少量氨气
⑥实验室用图2所示装置除去Cl2中的少量HCl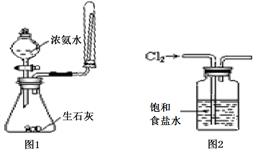
| A.③④⑥ | B.①②③ | C.④⑤⑥ | D.①③④⑤⑥⑩ |