下列各表述与示意图一致的是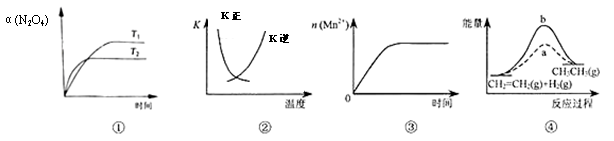
A.图①表示N2O4(g) 2NO2(g) ΔH>0,N2O4转化率随温度、时间的变化 2NO2(g) ΔH>0,N2O4转化率随温度、时间的变化 |
B.图②中曲线表示反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,正、逆反应的平衡常数K随温度的变化 2SO3(g) ΔH<0,正、逆反应的平衡常数K随温度的变化 |
| C.图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化 |
| D.图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g) |
下列各组离子能大量共存,且溶液为无色透明的是
| A.K+、S2-、NO3-、H+ | B.CrO42-、H+、K+、Cl- |
| C.Ba2+、Na+、HCO3-、OH- | D.K+、SO42-、S2-、Na+ |
在100g碳不完全燃烧所得气体中,CO占1/3,CO2占2/3,且C(s)+1/2O2(g)=CO(g);△H=-110.35kJ/mol
CO(g)+1/2O2(g)=CO2(g);△H="-282.57" kJ/mol,
与这些碳完全燃烧相比,损失的热量是
| A.392.92kJ | B.2489.44kJ | C.784.92kJ | D.3274.3kJ |
反应A(g)+3B(g)  2C(g)+2D(g)在四种不同情况下的反应速率,其中表示反应速率最快的是
2C(g)+2D(g)在四种不同情况下的反应速率,其中表示反应速率最快的是
A.v(A)=0.15 mol·L-1·min-1B.v(B)=0.02 mol·L-1·s-1
C.v(C)=0.40 mol·L-1·min-1D.v(D)=0.45 mol·L-1·min-1
下列变化中,属于放热反应的是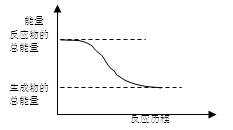
| A.H2O(g)==H2O(l) △H= -44kJ/mol |
| B.2HI(g)==H2(g)+I2(g) △H=+14.9kJ/mol |
| C.能量变化如图所示的化学反应 |
| D.形成化学键时放出能量的化学反应 |
C4H10的一氯取代物共有
| A.1种 | B.2种 | C.3种 | D.4种 |