在一个固定体积的密闭容器中,加入2mol A和1mol B发生反应:2A(g)+B(g) 3C(g)+D(g),达到平衡时,C的浓度为W mol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是
3C(g)+D(g),达到平衡时,C的浓度为W mol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是
| A.4molA+2molB | B.2molA+1molB+3molC+1molD |
| C.3molC+1molD+1molB | D.3molC+1molD |
下列关于有机物的说法中,正确的一组是()
①淀粉、油脂、蛋白质在一定条件下都能发生水解反应
②卤代烃大多数为液体或固体,可溶于水和大多数有机溶剂
③除去乙酸乙酯中残留的乙酸,加过量饱和碳酸钠溶液振荡后,静置分液
④石油的分馏和煤的干馏都是化学变化
⑤塑料、橡胶和纤维都是合成高分子材料
| A.①③ | B.②④ | C.①⑤ | D.③④ |
下列有关反应中所观察到的现象不正确的是()
| A.酸性高锰酸钾溶液与足量乙炔反应,溶液由紫色变成无色 |
| B.热的氧化铜加入乙醇中,乙醇由无色变成绿色 |
| C.苯酚钠浓溶液中滴加入稀盐酸,溶液由澄清变浑浊 |
| D.葡萄糖溶液与新制氢氧化铜共热,沉淀由蓝色变成红色 |
在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是()
A.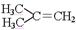 |
B.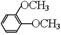 |
C.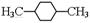 |
D.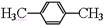 |
现 有两组混合液:①乙酸乙酯和乙酸钠溶液②乙醇和丁醇,分离以上各混合液的正确方法依次是()
有两组混合液:①乙酸乙酯和乙酸钠溶液②乙醇和丁醇,分离以上各混合液的正确方法依次是()
| A.分液、萃取 | B.萃取、蒸馏 |
| C.分液、蒸馏 | D.蒸馏、萃取 |
能通过化学反应使溴的四氯化碳溶液褪色的是()
| A.乙烯 | B.苯 | C.氯乙烷 | D.硬脂酸 |