下列离子方程式表达正确的是
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HCO3-+H2O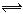 H3O++CO32- H3O++CO32- |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl- |
| D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O |
通过复习总结,你认为下列对化学知识概括合理的是
| A.物质中只要有阴离子存在就一定存在阳离子,有阳离子存在也一定有阴离子 |
| B.只由非金属元素组成的化合物不可能含有非极性共价键 |
| C.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |
下列说法正确的是
A.硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:
c (SO42-)> c (Na+)> c (NH4+)> c (OH-) =" c" (H+)
B.常温下0.4mol/LHB溶液 和0.2mol/LNaOH溶液等体积混合后溶液的PH=3则溶液中微粒浓度存在下面关系:c(HB)>c(Na+)>c(B-)> c(H+) >c(OH-)
C.在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液的PH< 7
D.用惰性电极电解含有一定浓度的CuSO4溶液,一段时间后需加入0.1molCu(OH)2才可以恢复至原来的浓度和体积,则在电解过程中转移了0.4mol电子
在一个容积固定的密闭容器中,发生反应:CO(g)+2H2(g)  CH3OH(g);ΔH<0。第2 min时只改变一个条件,反应情况如下表:
CH3OH(g);ΔH<0。第2 min时只改变一个条件,反应情况如下表:
| 时间 |
c(CO)/ mol/L |
c(H2)/mol/L |
c(CH3OH)/ mol/L |
| 起始 |
1 |
3 |
0 |
| 第2 min |
0.8 |
2.6 |
0.2 |
| 第4 min |
0.4 |
1.8 |
0.6 |
| 第6 min |
0.4 |
1.8 |
0.6 |
下列说法不正确的是
| A.第4 min至第6 min该化学反应处于平衡状态 |
| B.第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 |
| C.第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 |
| D.第6 min时,其他条件不变,如果升高温度,正反应速率增大 |
下列叙述不正确的是
| A.蔗糖、麦芽糖、淀粉溶液本身均不能发生银镜反应,但水解后均能发生银镜反应。 |
| B.铅蓄电池在放电过程中,负极、正极质量均增加。 |
| C.胶体能稳定存在的主要原因是同种胶粒带同种电荷。 |
| D.石油裂化的主要目的提高轻质油(如汽油)的产量。 |
有机物A是一种常用的内服止痛解热药。1 mol A 水解得到1 mol B 和1 mol 醋酸。A溶液具有酸性,不能使FeCl3溶液显色。A的相对分子质量不超过200。B分子中碳元素和氢元素总的质量分数为0.652。A、B都是有碳、氢、氧三种元素组成的芳香族化合物。则下列推断中,不正确的是
A.A、B的相对分子质量之差为42
B.B分子自身可发生缩聚反应生成高分子化合物
C.A的分子式是C7H6O3
D.B能与NaOH溶液、FeCl3溶液、溴水等物质反应