下列关于化学反应速率的说法正确的是( )
| A.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| B.化学反应速率为0.8mol/(L·s)是指1s时某物质的浓度为0.8mol/L |
| C.化学反应速率是指一定时间内反应物的物质的量减少或生成物的物质的量增加 |
| D.对于任何化学反应来说,反应速率越大,反应现象就越明显 |
下列各组溶液,在现有知识范围内只能通过焰色反应鉴别的是()
| A.NaNO3 KCl | B.Na2SO4 K2CO3 |
| C.KNO3 NaHSO4 | D.NaCl KCl |
某溶液中含有 、
、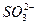 、
、 、CH3COO-四种离子,向其中加入足量的Na2O2固体,离子浓度基本保持不变的是(设溶液体积不变)( )
、CH3COO-四种离子,向其中加入足量的Na2O2固体,离子浓度基本保持不变的是(设溶液体积不变)( )
A. |
B.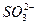 |
C.CH3COO- | D. |
含8.0 g NaOH的溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物7.9 g,则该无水物中一定含有的物质是()
| A.Na2S | B.NaHS | C.Na2S和NaHS | D.NaOH和NaHS |
某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是()
| A.30% | B. ×100% ×100% |
| C.26.5% | D.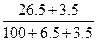 ×100% ×100% |
工业上常用氨碱法制取碳酸钠(将氨和二氧化碳先后通入饱和食盐水而析出小苏打,再经过滤、焙烧而得到纯碱),但却不能用氨碱法制碳酸钾,这是因为在溶液中()
| A.KHCO3溶解度较大 | B.KHCO3溶解度较小 |
| C.K2CO3溶解度较大 | D.K2CO3溶解度较小 |