如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置。则下列说法正确的是( )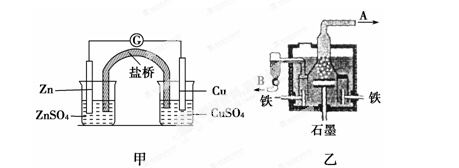
| A.甲装置中锌为负极,发生还原反应 |
| B.甲装置盐桥的作用是使反应过程中ZnSO4溶液和CuSO4溶液保持电中性 |
| C.乙装置中铁极为阳极,电极反应式为: 2Na++2e-=2Na |
| D.乙装置中B是氯气出口,A是钠出口 |
某学生用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(每次加入的盐酸的物质的量浓度相等),下列分析不正确的是()
| 盐酸 /mL |
50 |
50 |
50 |
| m(混合物)/g |
9.2 |
15.7 |
27.6 |
| V(CO2)(标况)/L |
2.24 |
3.36L |
3.36L |
A.盐酸的物质的量浓度为3.0mol/L
B.根据表中数据能计算混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量
D.15.7g混合物恰好与盐酸完全反应
将3.64g Fe2O3和Al2O3样品溶解在过量的200mL、pH=1的盐酸溶液中,然后向其中加入适量的NaOH溶液使Fe3+、Al3+ 刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为()
| A.0.1mol/L | B.0.2mol/L | C.0.4mol/L | D.0.8mol/L |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是()
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是()
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
| A.溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B.若溶液B选用浓硝酸,测得铜的质量分数偏小 |
| C.溶液A和溶液B选用稀硝酸 |
| D.实验室中方案Ⅱ更便于实施 |