设NA为阿伏加德罗常数的值,下列有关叙述正确的是 ( )
| A.28g乙烯所含共用电子对数目为4NA |
| B.0.5 mol 1, 3-丁二烯分子中含有C=C双键数为 NA |
| C.1 mol羟基所含的电子总数为10NA |
| D.标准状况下,11.2 L己烷所含分子数为0.5 NA |
从柑桔中炼制出有机物( ),下列有关它的推测不正确的是
),下列有关它的推测不正确的是
| A.分子式为C10H16 | B.常温下为液态,难溶于水 |
| C.它属于芳香烃 | D.1mol该物质与1molHCl加成所得产物有四种 |
有机化学中取代反应的范畴很广。下列4个反应中,不属于取代反应范畴的是
A.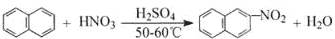 |
B. |
C. |
D. |
下列有机物的命名正确的是 





















| A. | 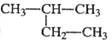 2-乙基丙烷 2-乙基丙烷 |
B. | CH 3-CH=CH-CH 32-丁烯 |
| C. |  3,4─二甲基戊烷 3,4─二甲基戊烷 |
D. | 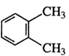 二甲基苯 二甲基苯 |
已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是
| A.N2H4+O2=N2+2H2O△H= —534.4kJ/mol |
| B.N2H4(g)+ O2(g)=N2(g)+2H2O(g)△H = —16.7kJ/mol |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H = —534.4kJ/mol |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H = —534.4kJ/mol |
在①甲烷②乙炔③丙烯④苯四种有机化合物中,分子内所有原子均在同一平面的是
| A.②③ | B.②④ | C.①③ | D.③④ |