下列反应既属于氧化还原反应,又是吸热反应的是
| A.铝片与稀盐酸的反应 | B.Ba(OH)2•8H2O与NH4Cl的反应 |
| C.灼热的炭与CO2的反应 | D.甲烷在氧气中的燃烧反应 |
下面有关铜的化合物的性质叙述中正确的是
| A.CuSO4变成CuSO4·5H2O是物理变化 |
| B.一定条件下,新制的Cu(OH)2浊液能与乙醛反应但不能与乙酸反应 |
| C.CuO是黑色固体,与水反应可生成Cu(OH)2 |
| D.Cu2O遇硝酸可能会被氧化成Cu2+ |
如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图。根据图示判断,下列结论中不正确的是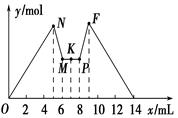
| A.N点时溶液中的溶质只有NaCl |
| B.M点之前加入的是NaOH溶液,M点之后加入的是盐酸 |
| C.c(NaOH)=c(HCl) |
| D.原混合溶液中c(MgCl2)∶c(AlCl3)=1∶1 |
在密闭容器中进行反应CH4(g)+H2O(g)  CO(g)+3H2(g);ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是
CO(g)+3H2(g);ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是
| A.0~5 min内,v(H2)=0.1 mol·(L·min)-1 |
| B.反应进行到12min时,CH4的转化率为25% |
| C.恒温下,缩小容器体积,平衡后H2浓度减小 |
| D.10 min时,改变的外界条件可能是升高温度 |
下列表示对应化学反应的离子方程式正确的是
①将过量SO2气体通入氨水中:SO2+ NH3·H2O = NH4+ + HSO3-
②用铁电极电解饱和食盐水:2Cl- + 2H2O  2OH- + H2↑+ Cl2↑
2OH- + H2↑+ Cl2↑
③向氢氧化钡溶液中逐滴加入少量碳酸氢钠溶液:Ba2++2OH-+2HCO3- = BaCO3↓+2H2O+ CO32-
④钢铁发生吸氧腐蚀正极的电极反应:2H2O + O2 + 4e-= 4OH-
⑤硝酸铁溶液中滴加足量HI溶液:Fe3+ + 3NO3-+12H+ +10I- = Fe2+ + 5I2 + 3NO↑ + 6H2O
| A.②③⑤ | B.①④⑤ | C.①③⑤ | D.②④⑤ |
某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4=2MnSO4+ 5Fe2(SO4)3+K2SO4+8H2O,盐桥中装有饱和K2SO4溶液。下列叙述中正确的是
| A.乙烧杯中发生还原反应 |
| B.甲烧杯中溶液的pH逐渐减小 |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.外电路的电流方向是从a到b |