除去下列物质中的少量杂质(括号内的物质为杂质),加入试剂或方法不正确的是
| A.NaCl溶液(BaCl2):加入足量Na2CO3溶液,过滤,再向滤液中加适量盐酸并加热 |
| B.KNO3溶液(AgNO3):加入足量KCl溶液,过滤 |
| C.NaCl固体(Na2CO3):加适量稀盐酸,加热蒸发 |
| D.CO2(HCl):将混合气体通过NaHCO3饱和溶液 |
科学家最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与金刚石的关系是
| A.同种物质 | B.同分异构体 | C.同位素 | D.同素异形体 |
已知:HCO3—+AlO2—+H2O=Al(OH)3↓+CO32—某溶液中可能含有OH−,CO32−,AlO2−,SiO32−,SO42−,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示,下列说法中不正确的是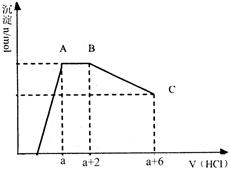
| A.原溶液肯定含有OH−,CO32−,AlO2−,SiO32− | B.K+和Na+至少含有其中一种 |
| C.n(CO32−):n(AlO2−)=3:2 | D.a值肯定大于4/3 |
肼(N2H4)—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。下列说法中,不正确的是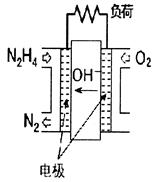
| A.该电池放电时,通入肼的一极为负极 |
| B.电池每释放1mol N2转移的电子数为4NA |
| C.通入空气的一极的电极反应式是:O2+2H2O+4e-=4OH- |
| D.电池工作一段时间后,电解质溶液的pH将不变 |
下列说法中,不正确的是
A.一次电池、二次电池和燃料电池是三种常见的化学电源
B.用石墨作电极电解氯化钠溶液:2Cl‒+2H2O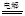 2OH‒+H2↑+Cl2↑
2OH‒+H2↑+Cl2↑
C.原降冰片二烯(NBD)经光照转化成为四环烷(Q):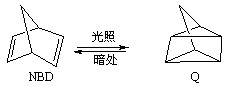 ,利用该反应可以贮存太阳能,则NBD的内能比Q的内能高
,利用该反应可以贮存太阳能,则NBD的内能比Q的内能高
D.一种“人工固氮”的新方法是在光照条件下,N2在催化剂表面与水蒸气发生反应生成NH3和氧气。己知:
| 化学键 |
N≡N |
H‒O |
N‒H |
O=O |
| 键能/kJ·mol-1 |
945 |
463 |
391 |
498 |
则“人工固氮”新方法的热化学方程式可表示为:
N2(g)+3H2O(g)  2NH3(g)+ 3/2O2(g);△H=+630kJ·mol-1
2NH3(g)+ 3/2O2(g);△H=+630kJ·mol-1
25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为
| A.12.5% | B.25% | C.50% | D.75% |