将2.0molPCl3,和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)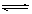 PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
| A.0.40mol | B.小于0.20mol | C.0.20mol | D.大于0.20mol,小于0.40mol |
下列离子方程式中,只能表示一个化学反应的是( )
①Fe+Cu2+===Fe2++Cu ②Ba2++2OH-+2H+ +SO===BaSO4↓+2H2O
+SO===BaSO4↓+2H2O
③Cl2+H2O===H++Cl-+HClO④CO+2H+===CO2↑+H2O ⑤Ag++Cl-===AgCl↓
| A.只有③ | B.②③ | C.③⑤ | D.①④ |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为: 3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl62 -+6M,关于该反应的说法中正确的组合是( )
-+6M,关于该反应的说法中正确的组合是( )
①氧化剂是H3AsO3;②还原性:Cl->As;③每生成1 mol As,反应中转移电子的物质的量为3 mol;④M为OH-;⑤SnCl62-是氧化产物。
| A.①③⑤ | B.①②④⑤ | C.①②③④ | D.只有①③ |
将质量分数为a%、物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使其质量分数为2a%.此时溶液的物质的量浓度为c2 mol·L-1.则c1和c2的关系是( )
| A.c1=2c2 | B.c2<2c1 |
| C.c2>2c1 | D.c2=2c1 |
一定温度下,mg某物质A在足量氧气中充分燃烧,使燃烧产物跟足量过氧化钠反应,过氧化钠质量增加了ng,且n=m,符合此要求的物质可能是( )
①H2②CO③H2和CO 的混合物④HCOOCH3⑤CH3CHO
的混合物④HCOOCH3⑤CH3CHO
A.⑤ |
B.只有①② | C.④⑤ | D.①②③④ |
Na2FeO4是一种高效多功能水处理剂.一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2===== 2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是( )
| A.Na2O2在上述反应中只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.Na2FeO4处理水时,既能杀菌,又能在处理水时产生胶体净水 |
| D.2 mol FeSO4发生反应时,共有10 mol电子发生转移 |