一定温度下的密闭容器中存在如下反应:
CO(g)+H2O(g) CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡_______,若未达到平衡,向哪个方向进行______。
(2)达到平衡时,CO的转化率____________________。
(3)当CO的起始浓度仍为2 mol·L-1,H2O(g)的起始浓度为6 mol·L-1,求平衡时CO的转化率_______。
将饱和FeCl3溶液滴入沸水中,液体变为________色,得到的是_________,用此分散系进行下列实验:
⑴将其装入U型管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色________,这说明________________,这种现象称为____________
⑵向其中加入饱和(NH4)2SO4溶液发生的现象是______________,原因是______________
⑶向其中滴入过量稀硫酸,现象是__________________________________________,其原因是______________________________________
对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的.
(1)现有下列6种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2.按照不同的分类标准,它们中有一种物质与其他5种有明显的不同,请找出这种物质,并写出依据(写出两种分类方法):
①____________________________________________________________________.
②____________________________________________________________________.
(2)从上述物质中分别找出两种能相互反应的物质,各写一个非氧化还原反应的方程式和氧化还原反应的方程式:______________________________________________________________________、______________________________________________________________________.
(3)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,请用简单的图示方法表示二者之间的关系:______________________.
(4)生活中的食醋和淀粉溶液分别属于分散系中的______和________,用________可以鉴别(填化学专用名词).
世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全灭菌消毒剂,ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,它在食品保鲜、饮用水消毒等方面有着广泛的应用。
(1)实验室制备ClO2的方法之一为:
2KClO3+H2C2O4+H2SO4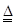 2ClO2↑+K2SO4+2CO2↑+2H2O(H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是________。
2ClO2↑+K2SO4+2CO2↑+2H2O(H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是________。
| A.KClO3在反应中得到电子 |
| B.ClO2是氧化产物 |
| C.H2C2O4在反应中被氧化 |
| D.1 mol KClO3参加反应有2 mol电子转移 |
(2)KClO3和浓盐酸在一定温度下反应也会生成绿黄色的二氧化氯。其变化可表示为2KClO3+4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O
①浓盐酸在反应中表现出来的性质是__________________________________________;
②已知每产生0.1 mol Cl2,则发生转移的电子的物质的量为0.2 mol。ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒后的还原产物是氯离子,则其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。
含有下列离子的五种溶液①Ag+ ②Mg2+ ③Fe2+ ④Al3+ ⑤Fe3+试回答下列问题:
(1)既能被氧化又能被还原的离子是(填离子符号,下同)
(2)向③中加入NaOH溶液,现象是有关化学方程式为
(3)加入过量NaOH溶液无沉淀的是__________________
(4)加铁粉溶液质量增重的是,溶液质量减轻的
(5)遇KSCN溶液呈红色的是
(6)能用来鉴别Cl–存在的离子是
由硫可得多硫化钠Na2Sx,x值一般为2~6,已知Na2Sx与NaClO反应的化学方程式如下: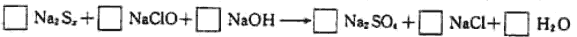
试配平上述方程式,若某多硫化钠在反应中消耗的NaClO和NaOH的物质的量之比为2:1,试以求得的x值写出该多硫化钠的分子式_________。