常温时,用1.0mol/L NaOH溶液中和某浓度硫酸溶液时,其pH 和所加NaOH溶液的体积关系如图所示。原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是
| A.1 mol/L 60mL | B.0.5 mol/L80mL |
| C.0.5 mol/L40mL | D.1 mol/L80mL |
取5mL 18mol/L的浓硫酸与足量的铜加热充分反应,等反应结束,收集到的是( )
| A.0.09mol的H2 | B.0.09mol的SO2 |
| C.小于0.045mol的SO2 | D.0.045mol的SO2 |
将铁粉、铜粉混合物加入FeC13溶液,充分反应后仍有固体存在,则
下列判断不正确的是 ( )
| A.加入KSCN溶液一定不变红色 | B.溶液中一定含Fe2+ |
| C.溶液中一定不含Cu2+ | D.剩余固体中一定含Cu |
两瓶均为棕黄色的氯化铁溶液和溴水,用下列试剂无法鉴别的是( )
| A.KSCN | B.CCl4 | C.NaOH | D.淀粉KI试纸 |
学生设计了如图的方法对A盐进行鉴定: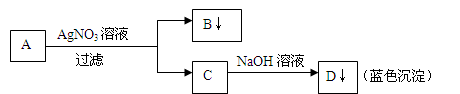
由此分析,下列结论中,正确的是( )
| A.A中一定有Fe3+ | B.C中一定有Cu2+ |
| C.B一定为AgBr沉淀 | D.A一定为CuCl2溶液 |
下列离子方程式书写正确的是( )
| A.氯气通入冷的氢氧化钠溶液中: Cl2 + 2OH-=Cl- + ClO- + H2O |
| B.铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| D.在氯化亚铁溶液中通入氯气:Cl2+Fe2+=Fe3++2Cl- |