“化学反应条件的控制是实验灵魂”。某校化学兴趣小组在老师指导下,探究了“影响过氧化氢分解速度的因素”。请你回答下列问题。
(1)取两支大试管,分别倒入适量的5%、10%的过氧化氢溶液,再加入等量的二氧化锰,各收集一小试管气体,发现浓度大的先收集满。该操作过程中合理的排列顺序 。(选填序号)
①检验装置的气密性 ②旋紧连有导管的单孔塞
③将水槽中待收集气体的小试管注满水 ④有连续稳定气泡再排水集气
⑤向大试管内倒入适量过氧化氢溶液再加入少许二氧化锰粉末
(2)取a 、b两支试管加入等体积5%的过氧化氢溶液,再分别加入少许二氧化锰粉末、氧化铜(CuO)粉末,发现a 中比b中产生气泡多且快。随即用带火星的木条分别悬空伸入试管内,发现a中火星复燃,b中火星仅发亮但不复燃。由此得出影响过氧化氢溶液分解的因素是 。
(3)某同学继续探究“红砖粉末是否也可以作过氧化氢分解的催化剂?”实验步骤和现象如下:
a b c d e f
①他分别向两支试管中加入等质量等浓度的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快。
②将反应较快的试管内固体过滤出来,洗涤、烘干。
③用烘干后的固体重复步骤①的实验,现象与步骤①完全相同。
试回答:步骤①中他除了选用试管外还用到上面列出的仪器有 (填字母)。步骤③的实验目的是 。该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来 。
2011年,日本福岛第一核电站发生核辐射泄漏,产生放射性碘-131,可能被附近居民吸入,引发甲状腺疾病或甲状腺癌。请回答下列问题:
(1)世界卫生组织提示要求谨慎服用碘片,以减少人体甲状腺吸收放射性碘。碘片的主要成分为碘化钾(化学式为KI),则碘化钾中碘元素化合价为。推荐服用量为每天100毫克碘元素(碘、钾的相对原子质量分别为127、39),某品牌碘片剂每颗含有10毫克碘化钾,则每天需要服用颗碘片剂。
(2)每500 g加碘食盐,经化验其中含有碘元素 50 mg,我们每天食用10 g碘盐,则我们从碘盐中可吸收mg碘元素,食用碘盐(能否)防治核辐射。
维生素C(简称Vc,又名抗坏血酸),易溶于水,易被氧化。人体缺乏Vc可能引发多种疾病。水果和蔬菜中含有丰富的Vc。某研究性学习小组对它探究如下:
探究一:测定饮料中Vc的含量。
【查阅资料】Vc能和高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有1 mL等浓度高锰酸钾稀溶液的四支试管中逐滴滴加果味饮料、苹果汁、梨汁和0.04%的Vc溶液,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
| 果味饮料 |
苹果汁 |
梨汁 |
0.04%的Vc溶液 |
|
| 滴加的滴数 |
40 |
10 |
20 |
5 |
【实验结论】分析数据可知,Vc含量最高的是,含量为(各液体密度上的差别和每一滴的体积差别忽略不计)。
探究二:蔬菜放置时间的长短对其Vc含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案:。
【实验结论】按上述方案实验,根据这一实验结果,分析得出蔬菜放置时间的长短对其Vc的含量有影响。
【实验反思】化学实验需要控制变量。下列情况不会影响到测定结果的是。
A.每次实验所用的果汁颜色不同
B.量取的被测物质的体积不同
C.试管的大小不同
D.没有用同一规格胶头滴管滴加
如图是某橙汁饮料标签上的部分内容:
| 配料:纯净水、白砂糖、 鲜橙浓缩汁、柠檬酸、 维生素C、食用香精、 鲜橙原汁含量>10% 净含量:500 mL |
(1)除配料中涉及的营养物质外,人体必需的营养物质还有、。
(2)该饮料的pH7(选填“大于”“小于”或“等于”)。
(3)如何检验一种无色溶液是否具有酸性?请设计两种实验方案:
方案一:实验步骤;
实验现象;
结论。
方案二:实验步骤;
实验现象;
结论。
铬是人体必需的微量元素之一,最近由于毒胶囊事件,引发对铬的关注。
(1)金属铬呈银白色,难溶于水,在空气中不易被氧化、耐腐蚀,在金属防锈上应用广泛。根据上述信息,写出金属铬的一种物理性质:。
(2)含铬物质的毒性与铬元素(Cr)的化合价有关。已知CrCl3中氯元素的化合价为-1价,则CrCl3中铬元素的化合价为:。
(3)如图表示人体生理机能与必需元素含量的关系。若长期摄入铬超标的食物和饮用水,会导致人体生理机能从最佳区向区移动,从而影响健康。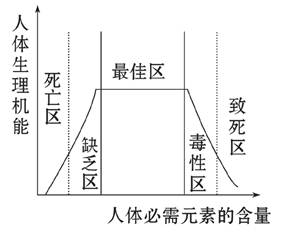
在人的胃液中,盐酸(HCl)的质量分数大约是0.45%~0.6%。它具有以下生理功能:①促进胃蛋白酶的催化作用,使蛋白质水解而被人体吸收;
②使糖类物质进一步水解;③杀菌。
请结合上述内容回答下列问题:
(1)如果用Al(OH)3的混合剂治疗胃酸过多,则发生反应的化学方程式为。
(2)人类食用适量的NaCl有利于。
| A.促进盐酸产生 | B.帮助消化和增进食欲 |
| C.治疗胃酸过多 | D.治疗缺碘性甲状腺肿大 |
(3)糖类、、油脂、维生素、无机盐和水是人体的六大营养物质。在这六大营养物质中,不经过消化,就可以在消化道内直接被人体吸收的有。