现有如下各说法:( )
①在水分子中氢、氧原子间以共价键相结合;
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键;
⑤冰的密度比水的密度小,这与氢键有关;
上述各种说法正确的是
| A.①②⑤ | B.①②④⑤ | C.①②③④⑤ | D.①③④⑤ |
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是
| A |
BaCl2与Na2SO4溶液 |
Ba(OH)2与H2SO4溶液 |
| B |
石灰石与硝酸反应 |
生石灰与盐酸 |
| C |
氢氧化钠与盐酸 |
氢氧化钠与硫酸氢钠 |
| D |
Na2CO3溶液与硝酸溶液 |
CaCO3与硝酸溶液 |
下列各组物质,不能反应的是
| A.硫酸钠溶液和氯化钡溶液 | B.铝片和硝酸汞溶液 |
| C.硝酸钠溶液和氯化钾溶液 | D.稀盐酸和碳酸钠溶液 |
如图所示实验操作正确的是
A. 收集氧气 收集氧气 |
B.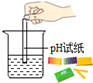 测溶液pH 测溶液pH |
C.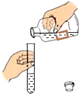 取用液体 取用液体 |
D.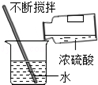 稀释浓硫酸 稀释浓硫酸 |
溶液、浊液、胶体三种分散系的本质区别为
| A.稳定性 | B.透明度 | C.分散质粒子的直径大小 | D.颜色 |
下列物质中,能够导电的电解质是
| A.Cu丝 | B.NaCl溶液 | C.熔融的MgCl2 | D.蔗糖 |