摩尔是( )
| A.国际单位制的一个基本物理量 | B.表示物质质量的单位 |
| C.计量微观粒子的物质的量的单位 | D.表示6.02×1023个粒子的集体 |
进行下列实验,由实验现象得出的结论错误的是()
| 选项 |
操作及现象 |
溶液可能是 |
| A |
通入CO2,溶液变浑浊。再升高至70℃,溶液变澄清。 |
C6H5ONa溶液 |
| B |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。 |
Na2SiO3溶液 |
| C |
通入CO2,溶液变浑浊。再加入品红溶液,红色褪去。 |
Ca(ClO)2溶液 |
| D |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊。 |
Ca(OH)2溶液 |
下列说法正确的是()
| A.有一澄清的碱性溶液,作离子鉴定时得出的结论是含有:AlO2-、Fe3+、HCO3- |
| B.某固体加入热NaOH溶液,生成使湿润红色石蕊试纸变蓝的气体,则固体中一定含有NH4+ |
| C.固体NaOH吸收了空气中的二氧化碳并溶于水后,则溶液中含较多的HCO3- |
| D.某溶液中加入BaCl2溶液出现不溶于稀HNO3的白色沉淀,则该溶液中一定含有SO42- |
用NA表示阿伏加德罗常数的数值,下列说法正确的是()
| A.lmol Na2O2晶体中共含有4NA个离子 |
| B.0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| C.常温常压下16gO2和O3混合气体含有NA个氧原子 |
| D.电解精炼铜时每转移NA个电子,阳极溶解32g铜 |
下列表示物质结构的化学用语或模型正确的是()
A.8个中子的氧原子的核素符号: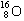 |
B.HF的电子式: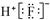 |
C.K+离子的结构示意图: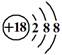 |
D.CH4分子的球棍模型: |
现有甲、乙两个实验,进行反应N2(g)+3H2(g)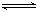 2NH3(g);丙、丁两个实验,进行反应H2(g)+I2(g)
2NH3(g);丙、丁两个实验,进行反应H2(g)+I2(g)  2HI(g) ∆H=-akJ•mol—1,实验条件和起始投料如下表所示,以下结论正确的是
2HI(g) ∆H=-akJ•mol—1,实验条件和起始投料如下表所示,以下结论正确的是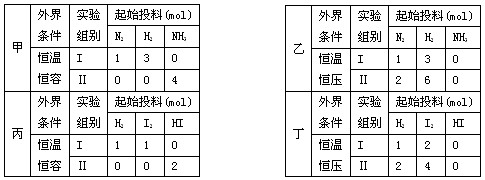
| A.甲组中,若平衡时N2和NN3的转化率分别为α1 和α2,则α1 +α2=1 |
| B.乙组中,平衡Ⅱ中NH3的浓度是平衡Ⅰ的二倍 |
| C.丙组中,若达平衡时Ⅰ中放热Q1kJ, Ⅱ中吸热Q2kJ,则Q1+Q2=a |
| D.丁组中,达平衡所需时间:Ⅰ小于Ⅱ |