对于密闭容器中的反应:2SO2(g)+O2(g) 2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是
2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是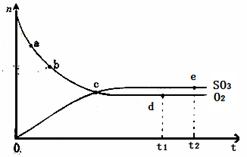
| A.点c处反应达到平衡 |
| B.点a的正反应速率比点b的大 |
| C.点d (t1时刻)和点e (t2时刻)处n(SO2)不一样 |
| D.其他条件不变,600℃时反应至t1时刻,n(SO 3)比上图中的d点值要大 |
下列各组顺序,正确的是( )
| A.微粒半径大小:S2- >Cl- >F- >Na+ >Al3+ |
| B.热稳定性大小:SiH4>PH3>NH3>H2O |
| C.沸点高低:HF>H2O>NH3 |
| D.等物质的量浓度溶液,酸性强弱顺序: H2SO4>H3PO4>H2SiO3>HNO2 |
下列说法正确的是()
| A.原子和其它原子形成共价键时,其共价键数一定等于该原子的价电子数 |
| B.HS-和HCl均是含有一个极性键的18电子粒子 |
| C.铵根离子呈正四面体结构 |
| D.离子化合物中只有离子键,共价化合物中只有共价键 |
因为镁、锂在元素周期表中具有特殊的“对角线”位置而性质相似,如它们的单质在过量氧气中燃烧均只生成正常氧化物等。以下叙述的锂的性质与镁相似,其中正确的是( )
| A.Li2SO4难溶于水 |
| B.LiOH是可溶于水,受热不分解的强碱 |
| C.遇浓H2SO4不会产生“钝化现象” |
D.Li2CO 3受热分解生成Li2O和CO2 3受热分解生成Li2O和CO2 |
短周期元素X、Y、Z、W在周期表 中的位置关系如图所示,下列叙述中正确的是()
中的位置关系如图所示,下列叙述中正确的是()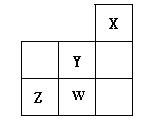
| A.Y的氢化物稳定性大于Z的氢化物稳定性 |
| B.Y的氢化物的水溶液是一种强酸 |
C.1molW的单质跟足量的NaOH水溶 液反应时,转移的电子数为1mol 液反应时,转移的电子数为1mol |
| D.X一定是活泼的非金属元素 |
水蒸气中常含有部分(H2O)2,要确定(H2O)2的存在,可采用的方法是()
| A.1L水蒸气冷凝后与足量金属钠反应,测量产生氢气的体积 |
B.1L水 蒸气通过浓硫酸后,测浓硫酸增重的质量 蒸气通过浓硫酸后,测浓硫酸增重的质量 |
| C.该水蒸气冷凝后,测水的PH |
| D.该水蒸气冷凝后,测氢氧原子比 |