N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)  4NO2 (g)+ O2(g) ΔH > 0
4NO2 (g)+ O2(g) ΔH > 0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s |
0 |
500 |
100 0 |
150 0 |
| c(N2O5)/ mol·L-1 |
5.00 |
3.52 |
2.50 |
2.50 |
下列说法中不正确的是
A.500 s内N2O5分解速率为2.96╳10-3mol·L-1·s-1
B.T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50%
C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
D.达平衡后其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)> 5.00 mol·L-1
下列化合物中,既显酸性,又能发生加成反应、氧化反应、酯化反应和消去反应的是( )
A.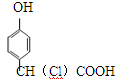 |
B.CH2(CHO)-CH2-CH(OH)-COOH |
| C.CH3—CH=CH—COOH | D.CH3CH(OH)CH2CHO |
某气态烃0.5mol能与1molHCl加成,转变为氯代烷烃,加成后产物分子上的氢原子又可被3molCl2完全取代,则该烃可能是()
| A.CH≡CH | B.CH≡CCH3 | C.CH3C≡CCH3 | D.CH2=CHCH3 |
由2氯丙烷制取少量的1,2丙二醇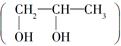 时,经过的反应依次为
时,经过的反应依次为
| A.加成→消去→取代 | B.消去→加成→水解 |
| C.取代→消去→加成 | D.消去→加成→消去 |
某醇和醛的混合物0.05 mol,能从足量的银氨溶液中还原出16.2 g银,已知该醇为饱和一元醇,该醛的组成符合CnH2nO,下列结论正确的是()
| A.此混合物中的醛一定是不甲醛 | B.此混合物中的醇、醛的物质的量之比是1︰1 |
| C.此混合物中的醛、醇可以是任意比 | D.此混合物中的醇、醛的物质的量之比是1∶3 |
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是
| A.CH3CH2CH3 | B.CH3 CH2COCH2CH3 |
| C.CH3CH2OH | D.CH3OCH3 |